
【题目】明代《天工开物》记载“火法”冶炼锌:“炉甘石十斤,装载入一泥罐内,…然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,…冷淀,毁罐取出,…,即倭铅也”(注:炉甘石的主要成分为碳酸锌,泥罐中掺有煤炭).下列说法不正确的是( )
A.倭铅是指金属锌和铅的混合物
B.煤炭中起作用的主要成分是C
C.我国历史上铅的使用早于锌
D.该冶炼锌的方法属于热还原法
科目:高中化学 来源: 题型:
【题目】乙酸橙花酯是一种食用香料,其结构简式如图,关于该有机物的叙述中不正确的是( ) 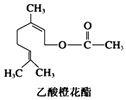
A.分子式为C12H20O2
B.1 mol该有机物水解时只能消耗1 mol NaOH
C.1mol该有机物可消耗3molH2
D.不能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是( )
A.若2CH3OH(1)+3O2(g)═2CO2(g)+2H2O(g)△H=﹣1478KJ/mol,则CH3OH(1)的燃烧热为739KJ/mol
B.若P4(白磷,s)═4P(红磷,s)△H<0,则红磷比白磷稳定
C.已知H+(aq)+OH﹣(aq)═H2O(1)△H=﹣57.3KJ/mol,则20.0g NaOH固体与稀盐酸完全中和,放出28.65KJ的热量
D.已知2C(s)+2O2(g)═2CO2(g)△H1; 2C(s)+O2(g)=2CO(g)△H2;△H1>△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中,所含原子数最多的是( )
A.8g O2
B.0.3mol NaCl
C.标准状况下4.48L CH4
D.含有3.01×1022个氧原子的H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A.在20℃,1.01×105Pa时,22.4L甲烷(CH4)所含的原子数为5NA
B.常温常压下,28g氮气所含的原子数为2NA
C.标准状况下,22.4L水所含有的分子数目为NA
D.0.5mol H2O所含的电子数目为9 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、都是金属,A中混有C时,在潮湿的空气中A先腐蚀,A与B组成原电池时,A为电池的正极。A、B、C三种金属的活动性顺序为
A. A>B>CB. A>C>BC. B>A>CD. B>C>A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)某温度下,纯水中的c(H+)=2.0×10﹣7mol/L,此时溶液的c(OH﹣)=mol/L;若温度不变,滴入稀盐酸使c(H+)=5.0×10﹣4mol/L,则溶液中,由水电离产生的c(H+)=mol/L,此时温度25℃(填“高于”、“低于”或“等于”).
(2)某温度下的水溶液中,C (H+)=10x mol/L,C (OH﹣)=10y mol/L,x和y的关系如图所示.计算:该温度下水的离子积为 . 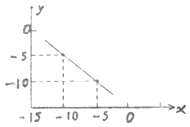
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)下列实验操作或对实验事实的描述不正确的是(填序号).
A.不宜用瓷坩埚灼烧氢氧化钠或碳酸钠
B.使用容量瓶配制溶液时,俯视刻度线定容后所得溶液浓度偏大
C.分液操作时,由于分液漏斗下端已沾满下层液体,故上层液体要从上口倒出
D.用托盘天平称量11.74g氯化钠晶体
E.用结晶法分离硝酸钾和氯化钠的混合物
(2)实验室需要0.1molL﹣1NaOH溶液450mL和0.5molL﹣1硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:
①如图1所示的仪器中配制溶液肯定不需要的是(填序号);配制上述溶液还需用到的玻璃仪器是(填仪器名称).
②下列操作中,容量瓶所不具备的功能有(填序号).
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.用来加热溶解固体溶质
③请计算需用托盘天平称取固体NaOH的质量为g.某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图2.由图中可以看出,烧杯的实际质量为g.
④根据计算得知,所需质量分数为98%、密度为1.84gcm﹣3的浓硫酸的体积为mL(计算结果保留一位小数).配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解饱和食盐水是一项重要的化学工业,请完成下列计算:
(1)当电解产生0.2mol NaOH时,能收集到标准状况下的H2L.
(2)已知室温时饱和食盐水的溶质质量分数为0.265,取200g饱和食盐水进行电解,当NaCl反应了一半时停止电解,①求写出所得混合溶液中NaCl的质量,②求出所得混合溶液中NaOH的质量分数.(写出计算过程,保留3位小数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com