
| A、Al2O3是一种难溶于水的氧化物 |
| B、Al2O3只与酸反应 |
| C、Al(OH)3既可以与酸反应又能与强碱反应 |
| D、Al(OH)3不溶于氨水 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 工业生产硫酸用水吸收SO3 | SO3可与水反应 | Ⅰ对,Ⅱ对,有 |
| B | Cl2与SO2混合后可漂白纸张 | Cl2和SO2有较好的漂白作用 | Ⅰ对,Ⅱ错,无 |
| C | 金属钠具有强还原性 | 高压钠灯发出透雾性强的黄光 | Ⅰ对,Ⅱ对,无 |
| D | 溴化银常用作感光材料 | 溴化银固体被保存在棕色细口瓶中 | Ⅰ对,Ⅱ对,有 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、54% | B、63% |
| C、9% | D、12% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、达到化学平衡时,若升高温度,则正反应速率减小,逆反应速率增大 |
| B、若单位时间内消耗x mol N2,同时生成2x mol NH3,则反应达到平衡状态 |
| C、达到平衡后,将容器体积减小为原来的一半,重新达到平衡后,c(NH3)变为原平衡时的2倍 |
| D、若达到平衡时,共放出46.2kJ热量,则有l mol NH3(g)生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、③④ | D、②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
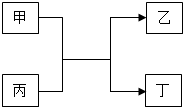 甲、乙、丙、丁四种物质的转化关系如图所示,其中甲、乙为单质,丙、丁为化合物.
甲、乙、丙、丁四种物质的转化关系如图所示,其中甲、乙为单质,丙、丁为化合物.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com