
【题目】S2Cl2用作橡胶的低温硫化剂和粘结剂,由硫与限量氯气在50~60℃反应制得,进一步氯化可得SCl2、S2Cl2、SCl2的某些性质如下:
水溶性 | 密度(g/cm3) | 颜色 | 熔点 | 沸点 | |
S2Cl2 | 空气中发烟雾,通水即分解 | 1.687 | 金黄色 | -76℃ | 138℃ |
SCl2 | 溶于水且剧烈反应 | 1.621 | 樱桃红 | -122℃ | 59℃ |
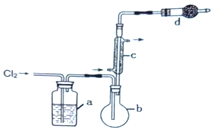
用如图所示装置制备S2Cl2回答下列问题:
(1)写出S2Cl2的电子式_________。
(2)写出仪器c的名称_________;实验开始前先在b中放入一定量的硫粉,加热使硫熔化,然后转动和摇动烧瓶使硫附着在烧瓶内壁形成一固体薄层,这样做的目的是_________。
(3)实验时,b装置需加热。最好采用何种方式加热_________。
(4)b中的反应开始前,需排除装置中的空气,简述相关操作:_________。
(5)装置d中盛放的试剂是_________;其作用是①_________②_________。
(6)为了获得更纯净的S2Cl2,需要对产品进行的操作是_________。
(7)若将S2Cl2放入水中同时产生沉淀和气体,写出反应的方程式_________。
【答案】 ![]() 直型冷凝管 增大反应接触面积 水浴加热 通Cl2一段时间后,看到黄绿色气体充满装置b后,再开始加热b 碱石灰 防止空气中的水蒸气进入d使产品与水反应 吸收剩余的Cl2 分馏(或蒸馏) 2S2Cl2+2H2O=SO2↑+3S↓+4HCl
直型冷凝管 增大反应接触面积 水浴加热 通Cl2一段时间后,看到黄绿色气体充满装置b后,再开始加热b 碱石灰 防止空气中的水蒸气进入d使产品与水反应 吸收剩余的Cl2 分馏(或蒸馏) 2S2Cl2+2H2O=SO2↑+3S↓+4HCl
【解析】根据氯原子成一键,硫原子成二键规律,该物质的电子式为![]() ;正确答案:
;正确答案:![]() ;起到冷凝作用的应该用球型冷凝管;正确答案:球型冷凝管;为了加快反应速度,硫形成薄层附着在烧瓶内壁,增大接触面积;正确答案:增大反应接触面积;
;起到冷凝作用的应该用球型冷凝管;正确答案:球型冷凝管;为了加快反应速度,硫形成薄层附着在烧瓶内壁,增大接触面积;正确答案:增大反应接触面积;
(3)硫与限量氯气在50~60℃反应制得,所以可以用水浴加热;正确答案:水浴加热;
(4)先通入Cl2一段时间后,看到黄绿色气体充满装置b后,排净了装置内的空气。再开始加热b ;正确答案:通Cl2一段时间后,看到黄绿色气体充满装置b后,再开始加热b;
(5)装置d中盛放的试剂是碱石灰,它既可以吸收反应剩余的氯气,同时防止外界中水蒸气进入b装置,因为S2Cl2在空气中发烟雾,通水即分解;正确答案:碱石灰 ;防止空气中的水蒸气进入d使产品与水反应;
(6)制得的S2Cl2中含有SCl2等杂质,二者沸点差别较大,可以采用蒸馏的方法进行分离,以获得更纯净的S2Cl2;正确答案:分馏(或蒸馏);
(7)若将S2Cl2放入水中同时产生单质硫沉淀和氯化氢气体;根据电子得失守恒规律,还会有另外一种气体二氧化硫生成;正确答案: 2S2Cl2+2H2O=SO2↑+3S↓+4HCl;


科目:高中化学 来源: 题型:
【题目】氢硫酸中存在电离平衡:H2S![]() H++HS-和HS-
H++HS-和HS-![]() H++S2-。已知酸式盐NaHS溶液呈碱性,若向10ml浓度为0.1mol/L的氢硫酸中加入以下物质,下列判断正确的是
H++S2-。已知酸式盐NaHS溶液呈碱性,若向10ml浓度为0.1mol/L的氢硫酸中加入以下物质,下列判断正确的是
A. 加水,会使平衡向右移动,溶液中氢离子浓度增大
B. 加入20ml浓度为0.1mol/L NaOH溶液,则c(Na+)=c(HS-)+c(H2S)+2c(S2-)
C. 通入过量SO2气体,平衡向左移动,溶液pH值始终增大
D. 加入10ml浓度为0.1mol/L NaOH溶液,则c(Na+)>c(HS-)>c(OH-)>c(H+)>c(S2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为验证SO2的还原性,特邀你参与以下探究活动。
I.理论预测
该兴趣小组实验实施前进行了充分的讨论交流,确定选择SO2和FeCl3溶液的反应来探究,并预测将SO2通入FeCl3溶液中的现象。小组同学想听听你的分析,你认为可能观察到的现象是:_____________,你预测的理论依据是(用离子方程式表示):________________________。
II.实验探究
(1)配制1mol/LFeCl3溶液(未用盐酸酸化)
①下面是小组四位同学在配制溶液时的“转移”操作,其中正确的是:_______________。
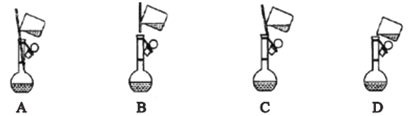
②测溶液的pH得知溶液呈酸性,其原因是:____________________ (用离子方程式表示)。
(2)SO2通入FeCl3溶液至饱和,观察到溶液由棕黄色变为红棕色,并没有观察到预期的现象。将反应后的溶液放置12小时后又出现了预期的结果。
查阅资料得知[Fe(HSO3)]2+为红棕色,生成[Fe(HSO3)]2+的反应为可逆反应。请你用化学方程式解释将SO2通入FeCl3溶液至饱和时观察到的现象:_______________。
(3)为了探究如何缩短红棕色变为预期颜色的时间,小组继续探究:另取少量FeCl3溶液,再通入SO2溶液变为红棕色,加浓HCl酸化,几分钟后变为预期颜色。
请你推测小组在实验方案设计中“加浓HC1酸化”的目的是:_______________。
III.感悟与分享
通过探究,小组同学深受启发、感悟良多。比如,有同学认为“实验才是化学的最高法庭”。请写出一种你的感悟与同学分享:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锑(Sb)及其化合物在工业上有许多用途。以辉锑矿(主要成分为Sb2S3,还含有PbS、As2S3、CuO、SiO2等)为原料制备金属锑的工艺流程如图所示:
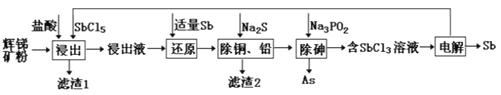
已知:①浸出液中除含过量盐酸和SbCl5之外,还含有SbCl3、PbCl2、AsCl3、CuCl2等;
②常温下:Ksp(CuS)=1.27×10-36,Ksp(PbS)=9.04×10-29;
③溶液中离子浓度小于等于1.0×10-5mol·L-1时,认为该离子沉淀完全。
(1)滤渣1中除了S之外,还有___________(填化学式)。
(2)“浸出”时,Sb2S3发生反应的化学方程式为_______________。
(3)“还原”时,被Sb还原的物质为___________(填化学式)。
(4)常温下,“除铜、铅”时,Cu2+和Pb2+均沉淀完全,此时溶液中的c(S2-)不低于_________;所加Na2S也不宜过多,其原因为_____________________________。
(5)“电解”时,被氧化的Sb元素与被还原的Sb元素的质量之比为_________。
(6)一种突破传统电池设计理念的镁-锑液态金属储能电池工作原理如图所示:
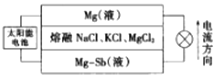
该电池由于密度的不同,在重力作用下分为三层,工作时中间层熔融盐的组成不变。充电时,Cl-向_____(填“上”或“下”)移动;放电时,负极的电极反应式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把1 L 0.1 mol/L的醋酸溶液用蒸馏水稀释到10 L,下列叙述正确的是( )
A. c(CH3COOH)变为原来的1/10
B. c(H+)变为原来的![]()
C. c(CH3COO-)/c(CH3COOH)的比值增大
D. 溶液的导电性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.道尔顿提出原子学说
B.侯德榜发明了“侯氏制碱法”,改进了碳酸钠的制取工艺
C.舍勒首次制得金属钠
D.门捷列夫提出元素周期表
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 氯水中有平衡:Cl2+H2O![]() HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅
HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅
B. 对CO(g)+NO2(g)![]() CO2(g)+NO(g),平衡体系增大压强可使颜色变深
CO2(g)+NO(g),平衡体系增大压强可使颜色变深
C. 对2NO2(g)![]() N2O4(g) △H<0, 升高温度平衡体系颜色变深
N2O4(g) △H<0, 升高温度平衡体系颜色变深
D. SO2催化氧化成SO3的反应,往往加入过量的空气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以石油裂解气为原料,通过一系列化学反应可得到重要的化工产品增塑剂G。流程如图所示
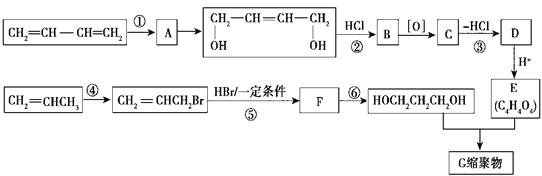
请完成下列各题:
(1)反应①发生的反应类型是 _________________。
(2)反应③发生的反应条件是 __________________。
(3)反应②、③的目的是 ________________________________________。
(4)写出反应⑤的化学方程式 ____________________________________________。
(5) B被氧化成C的过程中会有中间产物生成,该中间产物可能是 __________________(写出一种物质的结构简式),检验该物质存在的试剂是 _________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com