
| m |
| m |
| m |
| ρ |
| n |
| V |
| 12.1g |
| 242g/mol |
| 27.9g+12.1g |
| 1.2g/cm3 |
| 0.05mol |
| 0.033L |
| 20mL×1.51mol/L |
| 1mol/L |


科目:高中化学 来源: 题型:
| A、用试管加热液体时,所盛液体不超过容积的三分之一 |
| B、试剂瓶倾倒液体时,标签朝手心 |
| C、滴定时,眼睛注视滴定管中的液面 |
| D、称量时,腐蚀性固体药品要放在小烧杯或表面皿中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、遇FeCl3溶液显紫色或加入溴水产生白色沉淀,表示物质中可能含有酚羟基 |
| B、加入新制Cu(OH)2悬浊液并加热,有红色沉淀生成,或加入银氨溶液并水浴加热有银镜出现,说明该物质中含有-CHO |
| C、加入金属钠,有H2产生,表示物质可能有-OH或-COOH |
| D、加入NaHCO3溶液有气体放出或能使紫色石蕊试液变红,表示物质中含有-COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
 )具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是( )
)具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是( )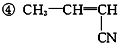 ⑤CH3-CH═CH2.
⑤CH3-CH═CH2.| A、③⑤ | B、②③ | C、①③ | D、④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com