
【题目】甲、乙、丙、丁分别是石蕊溶液、稀硫酸、碳酸钠溶液、澄清石灰水中的一种,若用四个圆表示四种溶液,两圆相交部分为两溶液混合后出现的主要实验现象,如下图所示.请回答:
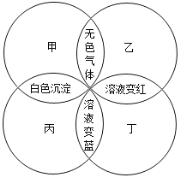
(1)丁是_________;通常其用途为_________。
(2)甲和丙的化学反应方程式为_________; 反应类型为_________。
【答案】
(1)石蕊溶液;作酸碱指示剂;
(2)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;复分解
【解析】
试题分析:(1)由于石蕊溶液是酸碱指示剂,遇到酸变成红色,遇到碱变成蓝色,再根据图示中丁与乙结合呈现红色,丁与丙结合呈现蓝色,所以丁是酸碱指示剂石蕊试液,所以乙是稀硫酸,因为硫酸与碳酸钠反应生成硫酸钠、水、二氧化碳,所以甲是碳酸钠溶液,丙就是氢氧化钙溶液,石蕊溶液是酸碱指示剂,遇到酸和碱呈现不同的颜色,可以用来判断溶液的酸碱性;故答案为:石蕊溶液;判断溶液的酸碱性;
(2)由上面的推断可知甲是碳酸钠,丙是氢氧化钙,所以该反应的反应物是碳酸钠和氢氧化钙,生成物是碳酸钙沉淀和氢氧化钠,用观察法配平,碳酸钙后面标上沉淀符号;两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应,该反应符合这一特点,属于复分解反应,故答案为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;复分解反应。


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
【题目】单质钛的机械强度高,抗腐蚀能力强,有“未来金属”之称。工业上常用硫酸分解钦铁矿(主要成分是钛酸亚锈FeTiO3)的方法来制取TiO2,再由TiO2制金属钛。主要反应有:
①FeTiO3 +3H2SO4=Ti(SO4)2+FeSO4+3H2O
②Ti(SO4)2+3H2O=H2TiO3↓+2H2SO4
③H2TiO3![]() TiO2+ H2O
TiO2+ H2O
④TiO2+2C+2Cl2![]() TiCl4+2CO
TiCl4+2CO
⑤TiCl4+2Mg![]() 2MgCl2+Ti。
2MgCl2+Ti。
下列叙述错误是( )
A.反应①属于非氧化还原反应 B.反应②属于非氧化迩原反应
C.反应④中TiO2是氧化剂 D.反应⑤表现了金属镁还原性比金属钛强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉堡包的制作原料有鸡胸肉、面包、鸡蛋、生菜等。下列说法正确的是
A. 生菜中的纤维素经消化分解可被人体吸收
B. 面包中的淀粉进入口腔先被酶催化水解为麦芽糖
C. 鸡蛋中的化合物含量最少的是糖类,最多的是蛋白质
D. 鸡胸肉中含有的动物多糖一一糖原可被人体直接吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生长在含盐量高、干旱土壤中的盐生植物,通过在液泡中贮存大量的Na+而促进细胞吸收水分,该现象说明液泡内的Na+参与( )
A. 调节渗透压 B. 组成体内化合物
C. 维持正常pH D. 提供能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.凡是铵盐都能与苛性钠共热产生NH3
B.NH4HCO3受热分解产生的气体经足量碱石灰干燥后可得到纯净的氨气
C.N2与O2在放电条件下化合属于氮的固定
D.工业硝酸略显黄色是由于里面含有Fe3+的缘故
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】V、W、X、Y、Z五种短周期元素的原子序数依次增大,在周期表中W与V、X相邻,Y与Z相邻,X、Y同主族,Z的单质可由其化合物发生反应制得,反应的离子方程式为
![]()
(1)上述反应中方框内的物质或离子为 (填化学式或离子符号)。
(2)Y、Z两种元素的简单离子的半径大小为 (用离子符号表示,半径用r表示)
(3)五种元素的最简单氢化物中,沸点最高的是 (填分子式),V、W、Y、Z四种元素的最高价含氧酸中有一种性质与其他三种不同,该酸的分子式为 。
(4)在催化剂作用下由VY2与Z2反应制得VZ4,该反应的化学方程式为VY2+Z2=VZ4+Y2Z2(未配平)。①写出上述反应的化学方程式: 。
②在Y2Z2分子中,Y与Z原子均满足8电子稳定结构,则Y2Z2的电子式为 。
(5)化合物ZnFe2Xa可作为新型纳米材料,常温下可将工业废气中的氧化物分解而除去。
![]()
若1mol ZnFe2Xa与YX2反应可生成0.75 mol Y,则a= ;1 mol ZnFe2Xa可分解物质的量之比为3:2的WX2、WX的混合气体的体积V= L(标准状况下)。
(6)Q与X同主族,位于第四周期,其原子序数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水晒盐后所得的苦卤中含有较高浓度的MgCl2、KCl以及金属溴化物。以下是苦卤化学分离的过程。
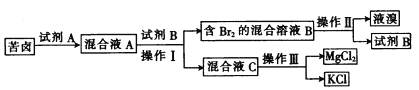
回答下列问题:
(1) 若试剂A是一种有色气体单质,则A是__________ (填化学式);写出该反应的离子方程式:___________。
(2) “操作II”是_______ (填“蒸发”“ 蒸馏”“ 分液”或“重结晶”,下同),“操作III”是________。
(3) 试剂B可能是下列物质中的________ (填字母)。
A.饱和NaCl溶液 B.CCl4 c.NaOH D.乙醇
实验室中也可用苯代替试剂B,但工业生产中,通常不使用苯,理由是____________________(任写两点)。
(4) MgCl2中可能含有NaCl杂质,检验杂质存在的方法是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com