
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:
| 步骤 | 操作 | 现象 |
| ① | 用pH试纸检验 | 溶液的pH大于7 |
| ② | 向溶液中滴加氯水,再加入CC14振荡,静置 | CC14层呈橙红色 |
| ③ | 取②的上层溶液,加入Ba(NO3)2溶液和稀HNO3 | 有白色沉淀产生 |
| ④ | 将③过滤,向滤液中加入AgNO3溶液和稀HNO3 | 有白色沉淀产生 |
| A、肯定含有的离子是①④⑤ |
| B、肯定没有的离子是②⑤⑦ |
| C、可能含有的离子是①②⑥ |
| D、不能确定的离子是①③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、两个反应中生成等量的I2时转移的电子数相等 |
| B、I2在反应①②中都是氧化产物 |
| C、NaI和NaIO3在一定条件下能反应生成I2 |
| D、NaIO3在任何化学反应中只能作氧化剂,不能作还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molCH4分子共价键总数为NA |
| B、含NA个Na+的Na2O2溶于1L水中,Na+的物质的量浓度为1mol/L |
| C、常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA |
| D、1molMg与足量O2或N2反应生成MgO或Mg3N2失去电子分别为2NA和3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O | ||||
| B、NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | ||||
C、用石墨电极电解氯化镁溶液:2Cl-+2H2O
| ||||
| D、铅蓄电池放电时的负极反应:PbSO4+2H2O-2e-═PbO2+4H++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 肉桂酸甲酯是调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精,用于肥皂、洗涤剂、风味剂和糕点的调味,在医药工业中作为有机合成的中间体.
肉桂酸甲酯是调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精,用于肥皂、洗涤剂、风味剂和糕点的调味,在医药工业中作为有机合成的中间体.

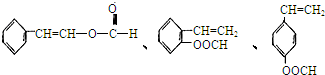
查看答案和解析>>
科目:高中化学 来源: 题型:
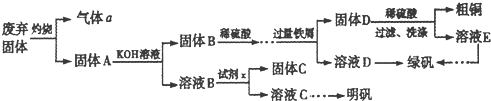
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com