
| A. | 用淀粉溶液检验溶液中是否存在碘离子 | |
| B. | 用分液漏斗分离水与乙醇的混合物 | |
| C. | 用氯化钡溶液鉴别碳酸钠溶液与硫酸钠溶液 | |
| D. | 用排饱和食盐水集气法收集氯气 |
分析 A.碘离子与淀粉不反应;
B.乙醇和水混溶;
C.氯化钡与碳酸钠、硫酸钠都生成沉淀;
D.氯气不溶于饱和食盐水.
解答 解:A.淀粉遇碘变蓝色,碘离子与淀粉不反应,故A错误;
B.乙醇和水混溶,不能用分液的方法分离,可用蒸馏的方法,故B错误;
C.氯化钡与碳酸钠、硫酸钠都生成沉淀,可加入盐酸鉴别,碳酸钠与盐酸生成二氧化碳气体,故C错误;
D.氯气不溶于饱和食盐水,可用排饱和食盐水集气法收集氯气,故D正确.
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及气体的收集、物质检验等知识点,把握实验操作的规范性、实验细节和实验原理为解答的关键,注意方案的合理性、评价性、操作性分析,难道不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| B. | 加入氢氧化钠溶液,先产生白色沉淀,后迅速变为灰绿色,最后变为红褐色,一定有Fe2+ | |
| C. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| D. | 加入硝酸银溶液产生白色沉淀,再加稀硝酸,白色沉淀不溶解,一定有Ag+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作 | 现象 | 结论 | |
| A. | 先滴加BaCl2溶液再滴加HCl溶液 | 生成白色沉淀 | 原溶液中有SO42- |
| B. | 先滴加稀盐酸再滴加AgNO3溶液 | 生成白色沉淀 | 原溶液中有Cl- |
| C. | 用洁净铁丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+ |
| D. | 滴加NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质熔点:Z>W | B. | 离子半径:X<Y | ||
| C. | 氧化物对应水化物的酸性:X>Z | D. | X和Z可存在于同一离子化合物中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
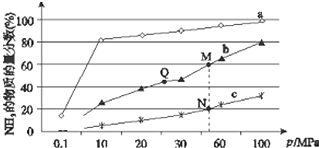 已知合成氨反应N2(g)+3H2?NH3(g)△H<0,当反应器中按n(N2):n(H2)=1:3投料后,在不同温度下,反应达到平衡时,得到混合物中NH3的物质的量分数随压强的变化曲线a、b、c如图所示.下列说法正确的是( )
已知合成氨反应N2(g)+3H2?NH3(g)△H<0,当反应器中按n(N2):n(H2)=1:3投料后,在不同温度下,反应达到平衡时,得到混合物中NH3的物质的量分数随压强的变化曲线a、b、c如图所示.下列说法正确的是( )| A. | 曲线a对应的反应温度最高 | |
| B. | 上图中M、N、Q点平衡常数K的大小关系为K(M)=K(Q)<K(N) | |
| C. | 相同压强下,投料相同,达到平衡所需时间关系为c>b>a | |
| D. | N点时c(NH3)=0.2 mol/L,则N点的c(N2):c(NH3)=1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
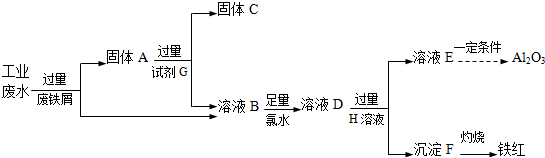
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2L一氧化碳和二氧化碳混合气体中含有的碳原子数目为0.5NA | |
| B. | 标准状况下,7.1克氯气与足量的氢氧化钠溶液反应转移的电子数位0.2NA | |
| C. | 92克二氧化氮和四氧化二氮的混合气体中含有的原子总数为6NA | |
| D. | 1.5mol/L氯化钙溶液中含有氯离子数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过量氨水与氯化铝溶液反应:Al3++3OH-═Al(OH)3↓ | |
| B. | 氢氧化铝溶于稀盐酸中:H++OH-═H2O | |
| C. | 氢氧化铝溶于氢氧化钠溶液:Al(OH)3+OH-═AlO2-+2H2O | |
| D. | 过量氢氧化钠溶液与氯化铝溶液反应:Al3++3OH-═Al(OH)3↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com