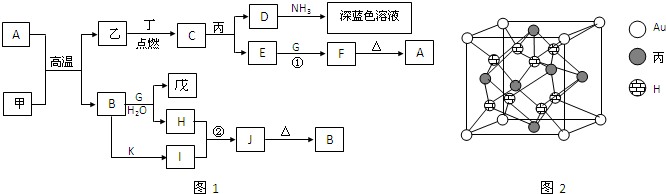
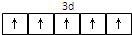
解答:解:由J的元素原子核内只有一个质子知J为H
2;I的焰色反应为黄色,所以I含Na元素;由金属B在A气体中燃烧产生棕黄色烟可知A为Cl
2,B为Fe或Cu,则D为FeCl
3或CuCl
2,;
且D+G+H
2O→H+I+J,结合I含Na元素知G为金属钠,且H
2O+G→K+J(H
2),所以K为NaOH,D的水溶液呈棕黄色,则D为FeCl
3,其水溶液与Na的反应为:6Na+2FeCl
3+6H
2O═2Fe(OH)
3↓+6NaCl+3H
2↑,F为无色、有刺激性气味气体,且能使品红溶液褪色,应为SO
2,则C为H
2SO
4,E为Fe
2(SO
4)
3,H为Fe(OH)
3,L为NaCl,
(1)由以上分析可知,K为NaOH,名称为氢氧化钠;所含化学键为离子键和共价键;故答案为:氢氧化钠;离子键、共价键;
(2))①D的水溶液呈棕黄色,D为FeCl
3,在氯化铁溶液中加入金属钠,钠先和水反应生成氢氧化钠和氢气,氢氧化钠和氯化铁反应生成氢氧化铁沉淀,则FeCl
3的水溶液与Na反应的离子方程式为:Fe
3++6H
2O+6Na=2Fe(OH)
3↓+6Na
++3H
2↑或2Na+2H
2O═2Na
++2OH
-+H
2↑,Fe
3++3OH
-=Fe(OH)
3↓,
故答案为:2Fe
3++6H
2O+6Na=2Fe(OH)
3↓+6Na
++3H
2↑或2Na+2H
2O═2Na
++2OH
-+H
2↑,Fe
3++3OH
-=Fe(OH)
3↓;
②少量B为Fe与C为H
2SO
4,少量铁在与浓硫酸在加热条件下反应生成硫酸铁和二氧化硫和水,反应的化学方程式为:2Fe+6H
2SO
4(浓)
Fe
2(SO
4)
3+3SO
2↑+6H
2O;
故答案为:2Fe+6H
2SO
4(浓)
Fe
2(SO
4)
3+3SO
2↑+6H
2O;
(3)①若将F为SO
2通入一定量K为NaOH的水溶液中,反应生成亚硫酸钠溶液,或亚硫酸氢钠溶液,或二者混合物,则所得溶液中各离子浓度一定满足的下列关系式为:
A.溶液中一定存在电荷守恒:c(Na
+)+c(H
+)=c(OH
-)+c(HSO
3-)+2c(SO
32-);溶液中一定存在电荷守恒,故A一定;
B.2c(Na
+)=3c(H
2SO
3)+3c(HSO
3-)+3c(SO
32-),生成的盐溶液是Na
2SO
3时物料守恒为c(Na
+)=2c(H
2SO
3)+2c(HSO
3-)+2c(SO
32-),若是NaHSO
3溶液存在物料守恒为:.c(Na
+)=c(H
2SO
3)+c(HSO
3-)+c(SO
32-),若是Na
2SO
3和NaHSO
3的混合溶液,存在的物料守恒为:2c(Na
+)=3c(H
2SO
3)+3c(HSO
3-)+3c(SO
32-);故B不一定;
C.c(Na
+)>c(HSO
3-)>c(SO
32-)>c(H
2SO
3),离子浓度大小是硫酸氢钠溶液中的离子浓度大小,若生成的是亚硫酸钠溶液时,离子浓度大小为:c(Na
+)>c(SO
32-)>c(HSO
3-)>c(H
2SO
3),故C不一定;
D.c(OH
-)>c(H
+)溶液中生成的盐溶液是Na
2SO
3,强碱弱酸盐水解显碱性,c(OH
-)>c(H
+);若是NaHSO
3,溶液中亚硫酸根离子电离程度大于亚硫酸氢根离子的水解,溶液呈酸性,c(OH
-)<c(H
+),故D不一定;
故答案为:A.
②若将标准状况下2.24L的SO
2通入150mL1mol?L
-1的NaOH溶液中.n(SO2)=0.1 mol;n(NaOH)=0.15mol;n(SO
2):n(NaOH)=2:3,反应后生成了亚硫酸钠和亚硫酸氢钠的混合溶液,反应的化学方程式为:2SO
2+3NaOH=Na
2SO
3+NaHSO
3+H
2O;则所得溶液中各粒子浓度关系满足的上述关系式:
A、一定符合溶液中的电荷守恒,故A符合;
B、Na
2SO
3和NaHSO
3的混合溶液,存在的物料守恒为:2c(Na
+)=3c(H
2SO
3)+3c(HSO
3-)+3c(SO
32-);故B符合;
C、反应得到的是同浓度的亚硫酸钠和亚硫酸氢钠的混合溶液,溶液中亚硫酸氢根离子电极程度大于亚硫酸根离子水解程度,故溶液显酸性,溶液中离子浓度大小为c(Na
+)>c(SO
32-)>c(HSO
3-)>c(H
2SO
3),故C不符合;
D、反应得到的是同浓度的亚硫酸钠和亚硫酸氢钠的混合溶液,溶液中亚硫酸氢根离子电极程度大于亚硫酸根离子水解程度,故溶液显酸性,c(OH
-)<c(H
+),故D不符合;
故答案为:AB.

 回答下列问题:
回答下列问题: