
已知元素X的基态原子最外层电子排布为nsn﹣1npn+2,则它最高价氧化物对应的水化物的酸根离子是( )
|
| A. | RO | B. | RO43﹣ | C. | RO | D. | RO32﹣ |
 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
在下列平衡2CrO42﹣(黄色)+2H+⇌Cr2O72﹣(橙红色)+H2O中,溶液介于黄和橙红色之间,今欲增加溶液的橙红色,则要在溶液中加入( )
|
| A. | H+ | B. | OH﹣ | C. | K+ | D. | H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用勒夏特列原理解释的是( )
|
| A. | 红棕色NO2加压后颜色先变深后变浅 |
|
| B. | 实验室中常用排饱和食盐水的方法收集氯气 |
|
| C. | SO2催化氧化成SO3的反应,使用过量的空气以提高二氧化硫的利用率 |
|
| D. | 压缩H2与I2(g)反应的平衡混合气体,颜色变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
二甲醚(CH3OCH3)被称为21世纪界的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能.工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g)⇌CH3OH(g)△H1=﹣90.7kJ•mol﹣1
②2CH3OH(g)⇌CH3OCH3(g)+H2O(g)△H2=﹣23.5kJ•mol﹣1
③CO(g)+H2O(g)⇌CO2(g)+H2(g)△H3=﹣41.2kJ•mol﹣1
(1)若要增大反应①中H2的转化率,在其它条件不变的情况下可以采取的措施为 .
A.加入某物质作催化剂 B.加入一定量CO C.反应温度降低 D.增大容器体积
(2)在某温度下,若反应①的起始浓度分别为:c(CO)=1mol/L,c(H2)=2mol/L,5min后达到平衡,CO的转化率为50%,则5min内CO的平均反应速率为 ;
若反应物的起始浓度分别为:c(CO)=4mol/L,c(H2)=a mol/L;达到平衡后,c(CH3OH)=2mol/L,
a= mol/L.
(3)催化反应室中总反应3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g)的△H= ﹣.
查看答案和解析>>
科目:高中化学 来源: 题型:
有四种混和溶液,分别由0.1mol/L CH3COONa溶液与等体积、等浓度的四种溶液混和而成:①HCl,②NaOH,③NaCl,④NaHCO3.关于混和后的溶液下列各项排序正确的是( )
|
| A. | pH:②>③>④>① | B. | c(CH3COO﹣):②>④>③>① |
|
| C. | c(H+):①>③>②>④ | D. | c(CH3COOH):①>④>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:
用铂作电极电解1000g 4.55% 的NaOH溶液,一段时间后,溶液中溶质的质量分数变为5.00%.则阳极产生的气体在标准状况下的体积为( )
|
| A. | 112L | B. | 56.0L | C. | 28.0L | D. | 168L |
查看答案和解析>>
科目:高中化学 来源: 题型:
我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法。
I.已知反应Fe2O3(s)+ CO(g)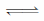 Fe(s)+ CO2(g) ΔH=-23.5kJ·mol-1,该反应在1000℃的平衡常数等于4。在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,应经过l0min后达到平衡。
Fe(s)+ CO2(g) ΔH=-23.5kJ·mol-1,该反应在1000℃的平衡常数等于4。在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,应经过l0min后达到平衡。
(1)CO的平衡转化率=____________
(2)欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是________。
a.提高反应温度
b.增大反应体系的压强
c.选取合适的催化剂
d.及时吸收或移出部分CO2
e.粉碎矿石,使其与平衡混合气体充分接触
Ⅱ.高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:CO(g)+ 2H2(g) 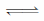 CH3OH(g)。请根据图示回答下列问题:
CH3OH(g)。请根据图示回答下列问题:
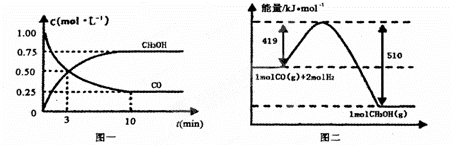
(3)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)=________。
(4)已知氢气的燃烧热286kJ/mol,请写出甲醇气体不充分燃烧的热化学方程式____________________________________________________________________。
(5)若在温度和容器相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡吋的有关数据如下表:
| 容器 | 反应物投入的量 | 反应物的 转化率 | CH3OH的浓度 | 能量变化 (Q1、Q2、Q3均大于0) |
| 甲 | 1mol CO和2mol H2 | α1 | c1 | 放出Q1kJ热量 |
| 乙 | 1mol CH3OH | α2 | c2 | 吸收Q2kJ热量 |
| 丙 | 2mol CO和4mol H2 | α3 | c3 | 放出Q3kJ热量 |
则下列关系正确的是________
A.c1=c2
B.2Q1=Q3
C.2α1=α3
D.α1+α2 =1
E.该反应若生成1mol CH3OH,则放出(Q1+Q2)kJ热量
Ⅲ.以甲烷为燃料的新型电池,其成本大大低于以氢为燃料的传统燃料电池,目前得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:

(6) B极上的电极反应式为 。
(7)若用该燃料电池做电源,用石墨做电极电解100mL 1mol/L的硫酸铜溶液,当两极收集到的气体体积相等时,理论上消耗的甲烷的体积为 (标况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
在pH都等于9的NaOH和CH3COONa两种溶液中,设由水电离产生的OH﹣离子浓度分别为amol/L与bmol/L,则A和B关系为( )
|
| A. | a>b | B. | a=10﹣4 b | C. | b=10﹣4 a | D. | a=b |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com