
A、 |
B、 |
C、 |
D、 |


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
| A、在稀氨水中滴加AgNO3溶液来配制银氨溶液,银氨溶液久置容易爆炸,要随配随用 |
| B、用标准NaOH溶液测定食醋中醋酸含量时应该使用酚酞作为指示剂 |
| C、将饱和氯水滴到淀粉碘化钾试纸上,如果试纸先变蓝后变白,说明氯水具有强氧化性 |
| D、重结晶法提纯KNO3产品除去少量NaCl时,应在较高温度下溶解产品配成浓溶液后冷却结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④ | B、②③ |
| C、②⑦ | D、④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实 验 操 作 及 现 象 | 实 验 结 论 |
| A | 将水蒸气通过灼热的铁粉,粉末变红褐色 | 铁与水在高温下发生反应 |
| B | 向某溶液中加入几滴新制的氯水,再加入2滴KSCN溶液,溶液变为红色 | 原溶液中不一定含有Fe2+ |
| C | 将某气体通入酸性高锰酸钾溶液中,溶液紫色褪去 | 该气体有还原性 |
| D | 用PH试纸测定NaClO溶液的酸碱性,试纸显蓝色 | NaClO水解显碱性 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
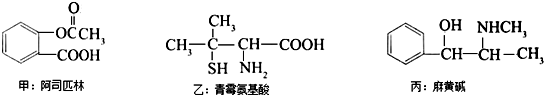
| A、都能发生酯化反应 |
| B、都能与NaOH反应 |
| C、甲的苯环上的一氯代物有4种 |
| D、丙的分子式为C10H15ON,苯环上的一氯代物有3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若生成1 molP(g),则放出的热量等于a kJ |
| B、若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| C、若升高温度,正反应速率加快,逆反应速率减慢,化学平衡正向移动 |
| D、达到化学平衡状态时,若c(Y)=0.100mol/L,则c(P)=0.0203 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
| 3%溴水 |
| 55℃ |
| 过量CaCO3 |
| 70℃ |
| 趁热过滤 |
| 乙醇 |
| 过滤 |
| 洗涤 |
| 干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④⑤ | B、②③④⑤ |
| C、③④⑤ | D、③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com