
分析 A.电荷不守恒;
B.二者反应生成硫酸钡、硫酸钠和水;
C.氯气足量溴离子、二价铁离子都被氧化;
D.次氯酸根离子具有强的氧化性能够氧化二氧化硫生成硫酸根离子;
E.二者反应生成碳酸钙、碳酸钠和水;
F.碳酸钙为沉淀,应保留化学式;
G.碳酸根离子分步水解,以第一步为主;
H.铝离子水解为可逆反应生成氢氧化铝少量,不标沉淀符号.
解答 A.制取NO的反应,离子方程式:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,故A错误;
B.氢氧化钡溶液中加入足量的硫酸氢钠溶液,离子方程式:Ba2++2OH-+2H++SO42-=BaSO4+2H2O,故B正确;
C.溴化亚铁溶液中通入足量的氯气,离子方程式:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-,故C错误;
D.少量二氧化硫通入次氯酸钠溶液中,离子方程式:SO2+3ClO-+H2O=SO42-+2HClO+Cl-,故D错误;
E.碳酸氢钙溶液与过量氢氧化钠溶液反应,离子方程式:Ca2++2HCO${\;}_{3}^{-}$+2OH-=CaCO3+2H2O+CO32-,故E正确;
F.厨房中用醋酸去除水垢(碳酸钙),离子方程式:CaCO3+2CH3COOH=CO2↑+H2O++Ca2++2CH3COO-,故F错误;
G.碳酸钠溶液中滴入酚酞溶液变红色,离子方程式:CO32-+H2O?HCO3-+H+,故G错误;
H.明矾净水,离子方程式:Al3++3H2O?Al(OH)3+3H+.故H错误;
故选:BE.
点评 本题考查了离子方程式的书写,明确发生反应的实质及离子方程式书写方法是解题关键,注意化学式拆分、注意反应物用量对反应的影响,题目难度不大.


科目:高中化学 来源: 题型:选择题
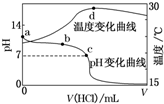 室温下,将1.000mol•L-1盐酸滴入20.00mL1.000mol•L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )
室温下,将1.000mol•L-1盐酸滴入20.00mL1.000mol•L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )| A. | a点由水电离出的c(H+)=1.0×10-14 mol•L-1 | |
| B. | b点:c(NH${\;}_{4}^{+}$)+c(NH3•H2O)=c(Cl-) | |
| C. | c点:c(Cl-)=c(NH${\;}_{4}^{+}$) | |
| D. | d点后,溶液温度略下降的主要原因是NH3•H2O电离吸热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从柑桔中可提炼出苧烯(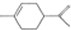 ),其分子式为C10H16,是1,3丁二烯的同系物 ),其分子式为C10H16,是1,3丁二烯的同系物 | |
| B. | 化学式为C4H10O的醇可被氧化成醛的有2种 | |
| C. | 2-氯丁烷(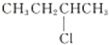 )与NaOH乙醇溶液共热发生消去反应的产物有2种 )与NaOH乙醇溶液共热发生消去反应的产物有2种 | |
| D. | 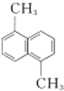 与 与 的一氯代物的数目不相等 的一氯代物的数目不相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 溶液 | 是否产生沉淀 | 沉淀成分 |
| ① | Ca(OH)2 | ||
| ② | BaCl2 | ||
| ③ | BaCl2和氨水 | ||
| ④ | BaCl2和氯水 | ||
| ⑤ | H2S | ||
| ⑥ | Ba(NO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 氧化剂 | I2的物质的量(mol) | 氧化剂 | I2的物质的量(mol) |
| H2O2 | IO3- | ||
| MnO4- | HNO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用填埋法处理未经分类的生活垃圾 | |
| B. | 用K2FeO4代替Cl2处理饮用水,既有杀菌消毒作用,又有净水作用 | |
| C. | 大量使用薪柴为燃料,践行低碳生活 | |
| D. | CO2、NO2或SO2的排放是形成酸雨的主要原因 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | $\frac{Vd}{MV+22400}$ | B. | $\frac{1000Vd}{MV+22400}$ | C. | $\frac{1000VdM}{MV+22400}$ | D. | $\frac{MV}{22.4(V+1)d}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com