
| A. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| B. | PM2.5(2.5微米以下的细颗粒物)主要来自化石燃料的燃烧 | |
| C. | 处理废水时加入明矾作为消毒剂对水进行杀菌消毒 | |
| D. | 某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为水中溶解了较多的CO2 |
分析 A.绿色化学又称环境友好化学,其核心就是利用化学原理从源头消除污染;
B.化石燃料的燃烧产生大量灰尘颗粒;
C.明矾中铝离子水解生成的氢氧化铝具有吸附性,能够净水,明矾不具有强氧化性,不能杀菌消毒;
D.空气中存在CO2溶于水使雨水显酸性,正常雨水的pH值约等于5.6;
解答 解:A.绿色化学的核心是利用化学原理从源头消灭污染,故A错误;
B.化石燃料的燃烧产生大量灰尘颗粒,是PM2.5(2.5微米以下的细颗粒物)主要来源,故B正确;
C.明矾能够净水,不能杀菌消毒,故C错误;
D.空气中存在CO2溶于水生成碳酸使雨水显酸性,正常雨水的pH值约等于5.6,雨水的pH值变小的原因是由于排放出来的SO2等气体溶于水后生成H2SO3,H2SO3随雨水的下降,逐渐被空气中的氧气所氧化生成易电离的H2SO4,故D错误;
故选:B.
点评 本题为综合题,题目难度不大,根据元素化合物的性质和相关概念分析解答,平时注意相关知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | Z的最高价氧化物的水化物能形成多种含Y元素的盐 | |
| B. | W的氧化物对应水化物的酸性一定强于Z | |
| C. | Y的单质应该保存在水中 | |
| D. | X的氢化物沸点比Z的氢化物沸点低 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
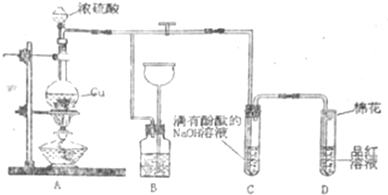
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
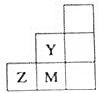
| A. | 非金属性:Y>Z>M | |
| B. | 离子半径:M->Z2->Y- | |
| C. | Z元素存在同素异形现象 | |
| D. | 三种元素中,Y的最高价氧化物对应的水化物酸性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L盐酸和0.1mol/L醋酸分别与0.2mol/L氢氧化钠溶液反应的速率相同 | |
| B. | 0.1mol/L盐酸和0.1mol/L硝酸分别与大小相同的大理石反应的速率相同 | |
| C. | 铝和铁分别与0.1mol/L硫酸的反应速率相同 | |
| D. | 大理石块与大理石粉末分别与0.1mol/L盐酸反应的速率相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
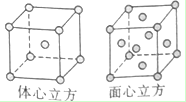 X、Y、Z、W为前四周期元素且原子序数依次增大,X的电子层数等于核外电子数,Y元素基态原子核外未成对电子数为2且X与Y形成的化合物在常温下为常见的液体R,Z元素原子最外电子层上s、p电子数相等,W基态原子3d轨道的电子数是4s轨道电子数的3倍.请回答下列问题:
X、Y、Z、W为前四周期元素且原子序数依次增大,X的电子层数等于核外电子数,Y元素基态原子核外未成对电子数为2且X与Y形成的化合物在常温下为常见的液体R,Z元素原子最外电子层上s、p电子数相等,W基态原子3d轨道的电子数是4s轨道电子数的3倍.请回答下列问题: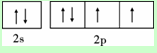 ,其第一电离能在同周期元素中由大到小排第4 位.
,其第一电离能在同周期元素中由大到小排第4 位.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com