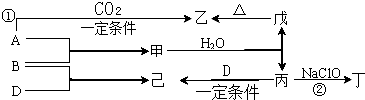
已知:A、B、D为中学常见的单质,只有一种是金属,对应的元素均处在周期表中的短周期;甲、乙、丙、丁、戊、己为短周期元素组成的化合物.其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,分子中不同原子的个数比为1:2,各原子最外层电子都达到稳定结构;乙是一种耐火材料;己是一种无色气体.各物质间的转化关系如图所示(某些条件已略去).请回答:
(1)单质B的组成元素在周期表中的位置是
.
(2)丁的电子式为
.
(3)反应①的化学方程式为
.
(4)丁的燃烧产物对环境无污染.丁-空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液.该电池放电时,通入丁的电极反应式是:
,电池工作一段时间后,电解质溶液的pH将
(填“增大”、“减小”、“不变”).
(5)反应②中,0.5mol NaClO参加反应时,转移1mol 电子,其化学方程式为:
.
(6)标准状况下用排水法收集满一烧瓶己(水蒸气不计),塞上带导管的橡皮塞,通过导管向其中缓慢通入氧气,现象是:
,一段时间后,常压下不能再通入氧气,则将烧瓶倒立,导管插入盛水的水槽中,用粘冰水的毛巾冷却烧瓶,即看到烧瓶中出现“喷泉”,“喷泉”结束时,瓶中溶液的物质的量浓度是:
.(精确到小数点后三位)


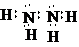 ,
,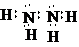 ;
;

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案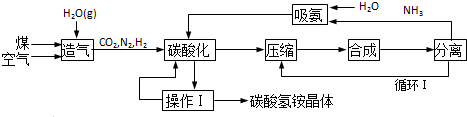
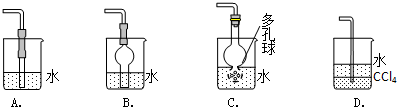


 用如图所示的收集装置收集氨气时,由于气流略强使得在试管底部形成气旋,导致氨气与空气混合而不能收集到纯氨气.现在有一小团棉花,请问将棉花放在试管那个位置可以阻止气旋?请说明理由.
用如图所示的收集装置收集氨气时,由于气流略强使得在试管底部形成气旋,导致氨气与空气混合而不能收集到纯氨气.现在有一小团棉花,请问将棉花放在试管那个位置可以阻止气旋?请说明理由.