
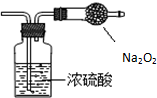
 某无色气体可能由O2、CO2、HCl、NH3、NO、Br2中的一种或几种组成,通过图中洗气瓶后气体体积减小,通过干燥管后(干燥管未与空气接触)气体呈红棕色,则下列推断正确的是( )
某无色气体可能由O2、CO2、HCl、NH3、NO、Br2中的一种或几种组成,通过图中洗气瓶后气体体积减小,通过干燥管后(干燥管未与空气接触)气体呈红棕色,则下列推断正确的是( )| A、原气体中一定有NO和O2 |
| B、原气体中一定有NO、CO2 |
| C、原混合气体中可能有HCl、Br2、O2 |
| D、原气体中一定没有HCl、Br2、CO2 |


 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源: 题型:
| A、苯的同系物命名必须以苯作为母体,其他的基团作为取代基 |
| B、二甲苯可以以邻、间、对这种习惯方法进行命名 |
| C、二甲苯也可以用系统方法进行命名 |
| D、化学式是C8H10的苯的同系物有4种同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、凡是中心原子采取sp3杂化的分子,其立体构形都是正四面体 |
| B、CH4分子中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合起来而形成的 |
| C、杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对 |
| D、凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蒸发 | B、萃取 | C、过滤 | D、蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解时,石墨做阴极,铁作阳极 |
| B、电解时,在阳极上产生氢气 |
| C、电解后得到KIO3产品的步骤有:过滤→浓缩→结晶→灼烧 |
| D、电解中,每转移0.6mol电子,理论上可得到0.1mol无水KIO3晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4-甲基-2-乙基戊烷 |
| B、2,5-二甲基己烷 |
| C、2,4-二甲基己烷 |
| D、2-乙基-4-甲基戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| I1/kJ?mol-1 | I2/kJ?mol-1 | I3/kJ?mol-1 | I4/kJ?mol-1 | I5/kJ?mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com