
| A、乙醇稀溶液:K+、Na+、SO42-、OH- | ||
| B、氨水溶液:Mg2+、Ag+、NO3-、CH3COOH | ||
C、
| ||
| D、使石蕊变红的溶液:Fe2+、Al3+、ClO-、CO32- |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(3b+0.5a)mol |
| B、(4b+0.5a)mol |
| C、(3b+1.5a)mol |
| D、无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可能是Al3+,也可能是Mg2+ |
| B、只能是Al3+ |
| C、只能是Mg2+ |
| D、以上说法都不对 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2通入水中:Cl2+H2O?2H++Cl-+C1O- | ||||
| B、钢铁发生吸氧腐蚀时,铁作负极:Fe-3e-=Fe3+ | ||||
| C、向双氧水中加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2O | ||||
D、用铜作阳极电解CuSO4溶液:2Cu2++2H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
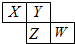 如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若w原子最外层电子数是其内层电子数的
如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若w原子最外层电子数是其内层电子数的| 7 |
| 10 |
| A、XY2和ZY2都是造成酸雨的主要因素 |
| B、Y元素的两种同素异形体在常温下都是气体 |
| C、最高价氧化物对应水化物的酸性W>Z |
| D、氢化物的沸点:HnZ 高于HnY |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某地区使用含较多Ca2+、Mg2+的天然水按下列步骤制取纯净水.
某地区使用含较多Ca2+、Mg2+的天然水按下列步骤制取纯净水.| ①沉降 |
| ②过滤 |
| ③曝气 |
| ④离子交换 |
| ⑤消毒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com