
在一定条件下,将PCl3(g)和Cl2(g)充入体积不变的的2L密闭容器中发生下述反应:PCl3(g)+Cl2(g)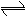
 PCl5(g);5min末达到平衡,有关数据如下表。
PCl5(g);5min末达到平衡,有关数据如下表。
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度(mol/L) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol/L) | C1 | C2 | 0.4 |
下列判断不正确的是
当反应达到平衡状态,容器中Cl2为1.2mol
反应5min内,V(PCl3)=0.08mol/(L·min)
达到平衡后再向容器中充入少量PCl5(g),混合气体的平均摩尔质量将变小。
平衡后移走2.0molPCl3和1.0molCl2,在相同条件下再达到平衡时,C(PCl5)<0.2mol/L
科目:高中化学 来源: 题型:
某合作学习小组讨论辨析以下说法,其中正确的是 ( )
①粗盐和酸雨都是混合物 ②沼气和水煤气都是可再生能源 ③冰和干冰既是纯净物又是化合物 ④不锈钢和目前流通的硬币都是合金 ⑤纯碱和熟石灰都是碱 ⑥豆浆和雾都是胶体
A.①②③④ B.①②⑤⑥
C.③⑤⑥ D.①③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
对于电解质的导电能力,下列说法正确的是 ( )
A.强电解质溶液的导电能力一定比弱电解质溶液的导电能力强
B.导电能力强的溶液一定是浓溶液
C.相同温度下,导电能力强的溶液中离子个数一定多
D.相同的温度下,单位体积中的离子个数越多,阴离子或阳离子所带电荷的绝对值越大,溶液的导电能力越强
查看答案和解析>>
科目:高中化学 来源: 题型:
已知 2Fe3+ +2I- =2Fe2+ +I2 2Fe2+ +Cl2 =2Fe3+ +2Cl- 则有关离子的还原性由强到弱的顺序为 ( )
A.Cl->Fe2+>I- B. Fe2+>I->Cl- C.I->Fe2+>Cl- D.Fe2+>Cl->I-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对有关物质性质的分析正确的是
A.IBr可与水反应生成HIO和HBr
B.在高温下用氢气还原MgCl2可制取金属镁
C.Na久置于空气中,最终生成NaHCO3
D.打开盛浓盐酸的试剂瓶可看到白色的雾,说明HCl不稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)某科研小组研究在恒温、恒容(容器容积为2L)下反应:N2(g)+3H2(g)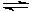 2NH3(g)的变化。初始条件n(H2)=3mol、n(N2)=1mol,反应达到平衡时H2的转化率为60%,NH3的体积分数为a%。
2NH3(g)的变化。初始条件n(H2)=3mol、n(N2)=1mol,反应达到平衡时H2的转化率为60%,NH3的体积分数为a%。
①此条件下反应的平衡常数K=
②若初始条件为n(H2)=n(N2)=0mol、n(NH3)=2.0mol,反应达到平衡时NH3的转化率为
③若初始条件为n(H2)=6mol、n(N2)=2mol,反应达到平衡时NH3的体积分数 a%(填“>”、“<”、或“=”)。
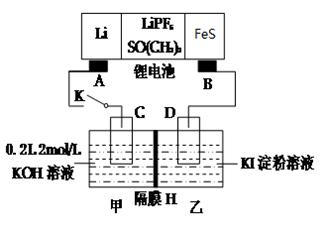
(2)锂电池广泛使用于手表、照相机等电子产品中,具有稳定性好、轻便、环保等优点。右图是以锂电池为电源的电解槽。
①LiPF6作为电池的电解质,可传导Li+导电,已知电池反应为FeS+2Li=Fe+Li2S则A为锂电池的 极,该锂电池的正极反应为 。
②隔膜H为阳离子交换膜,若电解结束后,甲中产生的气体在标准状况下的体积为4.48L,则隔膜H中通过的离子数目为 ,甲中溶液的浓度为 (假设溶液体积不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
氰气的化学式为(CN)2,它的性质和卤素相似,称为拟卤素,对其性质和有关化合物性质的叙述不正确的是( )
A.NaCN 和AgCN都易溶于水 B.HCl和HCN都易形成白雾
C.MnO2可与HCN反应生成(CN)2
D.(CN)2和NaOH溶液反应生成NaCN、NaCNO和H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
现将35g锌粉与少量浓硫酸在加热条件下充分反应,共收集到混合气体11.2L(标准状况),其质量为19.6g,则过剩的锌粉的质量为( )
A.1.0g B.2.0g C.2.5g D.3.5g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com