
| A. | 新型材料聚酯纤维、光导纤维都属于有机高分子 | |
| B. | 酸性高锰酸钾溶液应装在酸式滴定管中,原因是酸性高锰酸钾能氧化橡胶 | |
| C. | 植物油和裂化汽油都能使溴水褪色,原理是不同的 | |
| D. | 明矾能够用于净水,是因为明矾的溶液是酸性的 |
分析 A.光导纤维的主要成分为二氧化硅;
B.高锰酸钾具有强氧化性;
C.植物油和裂化气哟都含有碳碳双键;
D.明矾可水解生成具有吸附性的氢氧化铝胶体.
解答 解:A.光导纤维的主要成分为二氧化硅,为无机物不是高分子化合物,故A错误;
B.高锰酸钾具有强氧化性,可氧化橡胶管,应用酸性滴定管,故B正确;
C.植物油和裂化气哟都含有碳碳双键,都可与溴水发生加成反应,故C错误;
D.明矾可水解生成具有吸附性的氢氧化铝胶体,用于净水与酸性无关,故D错误;
故选B.
点评 本题综合考查元素化合物知识,侧重于化学与生活、生产的考查,为高考常见题型,有利于培养学生良好的科学素养,提高学习的积极性,难度不大,注意相关基础知识的积累.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 1 mol氢的质量是1 g | B. | 1 mol CO的质量为28 g•mol-1 | ||
| C. | 阿伏加德罗常数等于6.02×1023 | D. | 3.01×1023个SO2分子约是0.5 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用Na2O2作潜水器的供氧剂 | |
| B. | 自来水厂可用明矾对水进行消毒杀菌 | |
| C. | 锅炉水垢中的CaSO4可用Na2CO3溶液浸泡后再用酸清洗 | |
| D. | 工业制取粗硅是高温下用C还原SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 是烃 | B. | 不能在空气中燃烧 | ||
| C. | 常温下呈固态 | D. | 可能发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,无K+ | |
| B. | 因Cl2的氧化性强于I2的氧化性,所以置换反应I2+2NaClO3═2NaIO3+Cl2不能发生 | |
| C. | 反应3NO2+H2O═2HNO3+NO中氧化剂和还原剂的物质的量之比是3:1 | |
| D. | 在反应CaH2+2H2O═Ca(OH)2+2H2↑中,水作氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
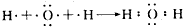 .
.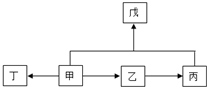 (3)A、B、C三种元素能形成多种化合物.某化合物甲一分子中含有一个氧原子,相对分子质量为46,其存在如图转化关系:
(3)A、B、C三种元素能形成多种化合物.某化合物甲一分子中含有一个氧原子,相对分子质量为46,其存在如图转化关系: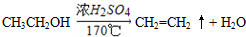 ;
;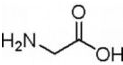 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若w原子最外层电子数是其内层电子数的$\frac{7}{10}$,则下列说法中不正确的是( )
如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若w原子最外层电子数是其内层电子数的$\frac{7}{10}$,则下列说法中不正确的是( )| A. | Y元素的两种同素异形体在常温下都是气体 | |
| B. | 原子半径由大到小排列顺序Z>Y>X | |
| C. | 最高价氧化物对应水化物的酸性W>Z | |
| D. | 阴离子半径由大到小排列顺序X>Y>Z>W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1 pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) | |
| B. | 常温下,pH=2的CH3COOH溶液和H2SO4溶液、pH=12的氨水和NaOH溶液,四种溶液中由水电离出的c(H+)不相等 | |
| C. | 常温下将浓度为0.1 mol•L-1的HF溶液加水不断稀释,溶液中$\frac{c({H}^{+})}{c(HF)}$的值始终保持增大 | |
| D. | 常温下0.1 mol•L-1的下列溶液①NH4Fe(SO4)2 ②NH4Cl ③NH3•H2O ④CH3COONH4中,c(NH4+)由大到小的顺序是:②>①>④>③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com