
如图:横坐标为溶液的pH值,纵坐标为Zn2+离子或Zn(OH)42-离子(配离子)物质的量浓度的对数,回答下列问题.
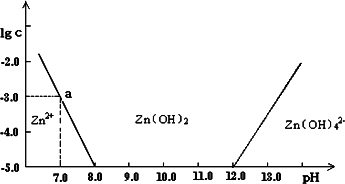
(1)往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为___________
(2)从图中a点数据计算可得Zn(OH)2的溶度积Ksp值为___________.
(3)某废液中含Zn2+离子,为提取Zn2+离子可以控制溶液中pH值的范围是_____.
(4)往1 L 1.00 mol/L ZnCl2溶液中加入NaOH固体至pH=6,根据(2)中求得的Ksp值或根据图像中的关系,可求得需NaOH________mol.
 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
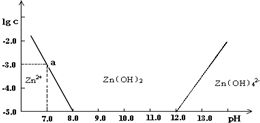 常温下二价锌在水溶液中的存在形式与pH的关系如图,横坐标为溶液的pH,纵坐标为Zn2+ 或Zn(OH)42-(配离子)物质的量浓度的对数(假设Zn2+离子浓度为10-5mol?L-1时,Zn2+离子已沉淀完全).下列说法正确的是( )
常温下二价锌在水溶液中的存在形式与pH的关系如图,横坐标为溶液的pH,纵坐标为Zn2+ 或Zn(OH)42-(配离子)物质的量浓度的对数(假设Zn2+离子浓度为10-5mol?L-1时,Zn2+离子已沉淀完全).下列说法正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:

(1)往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为____________。
(2)从图中数据计算可得Zn(OH)2的溶度积(Ksp)=___________。
(3)某废液中含Zn2+离子,为提取Zn2+离子可以控制溶液中pH的范围是____________。
(4)往
(5)已知:往ZnCl2溶液中加入硝酸铅或醋酸铅溶液可以制得PbCl2白色晶体;
c(HCl)/mol·L-1 | 0.50 | 1.00 | 2.04 | 2.90 | 4.02 | 5.16 | 5.78 |
c(PbCl2)/mol·L-1×10-3 | 5.10 | 4.91 | 5.21 | 5.90 | 7.48 | 10.81 | 14.01 |
根据上表数据判断下列说法正确的是___________(填字母序号)。
A.随着盐酸浓度的增大,PbCl2固体的溶解度先变小后又变大
B.PbCl2固体在0.50 mol·L—1盐酸中的溶解度小于在纯水中的溶解度
C.PbCl2能与浓盐酸反应生成一种难电离的阴离子(如配合离子)
D.PbCl2固体可溶于饱和食盐水
查看答案和解析>>
科目:高中化学 来源:2012届浙江省杭州外国语学校高二年级下学期期中考试化学试卷 题型:选择题
已知锌及其化合物的性质与铝及其化合物相似。如图,横坐标为溶液的pH,纵坐标为Zn2+离子或[Zn(OH)4]2-离子的物质的量浓度(假设Zn2+离子浓度为10-5mol·L-1时,Zn2+离子已沉淀完全)。下列说法不正确的是
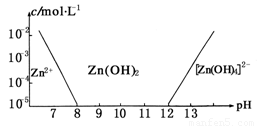
A.往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为:
Zn2++4OH-=[Zn(OH)4]2-
B.从图中数据计算可得Zn(OH)2的溶度积Ksp=10-17
C.某废液中含Zn2+离子,沉淀Zn2+离子可以控制溶液pH的范围是8~12
D.向1 L 1 mol·L-1ZnCl2溶液中加入NaOH固体至pH=6,需NaOH 0.2 mol
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
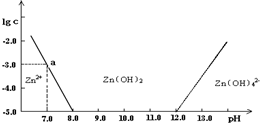
| A.从图中数据计算可得Zn(OH)2的溶度积Ksp=10-17 |
| B.pH<12的溶液中不存在Zn(OH)42- |
| C.某废液中含Zn2+离子,沉淀Zn2+离子可以控制溶液pH的范围是8~12 |
| D.向1L 1mol?L-1ZnC12溶液中加入NaOH固体至pH=7,需NaOH 2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
(11分)如图:横坐标为溶液的pH值,纵坐标为Zn2+ 离子或Zn(OH)42-离子(配离子)物质的量浓度的对数,回答下列问题。
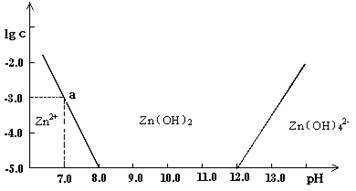
(1)往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为
。
(2)从图中a点数据计算可得Zn(OH)2的溶度积K sp值为 。
(3)某废液中含Zn2+ 离子,为提取Zn2+离子可以控制溶液中pH值的范围是 。
(4)往1L 1.00 mol/L ZnCl2溶液中加入NaOH固体至pH=6,根据(2)中求得的K sp值或根据图像中的关系,可求得需NaOH mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com