
| A. | 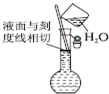 配制一定物质的量浓度溶液 | |
| B. | 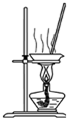 蒸干氯化锰溶液制MnCl2•4H2O | |
| C. | 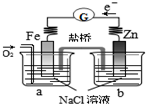 验证牺牲阳极的阴极保护,在a烧杯中滴入K3[Fe(CN)6]溶液,无蓝色沉淀产生 | |
| D. |  萃取时振荡溶液 |
分析 A.定容时使用胶头滴管;
B.蒸干氯化锰溶液时HCl挥发,得不到晶体;
C.若含亚铁离子,发生3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓(蓝色),牺牲阳极的阴极保护中Fe为正极;
D.振荡方法错误,应上下颠倒振荡.
解答 解:A.定容时使用胶头滴管,加液体至刻度线1-2cm处改用胶头滴管滴加,故A错误;
B.蒸干氯化锰溶液时HCl挥发,得不到晶体,应利用蒸发浓缩、冷却结晶法,故B错误;
C.图中Fe为正极,则Fe不能失去电子,在a烧杯中滴入K3[Fe(CN)6]溶液,无蓝色沉淀产生,可验证牺牲阳极的阴极保护,故C正确;
D.振荡应上下颠倒,左手托住,右手食指和中支按住塞子,该操作不合理,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握溶液配制、原电池、盐类水解及实验基本操作等为解答的关键,侧重分析与实验能力的考查,注意实验评价性分析,题目难度不大.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
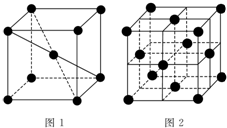 1 183K以下纯铁晶体的基本结构单元如图1所示,1 183K以上转变为图2所示结构的基本结构单元,在1中铁原子的配位数为8;其中为密堆积的是2(填“1”或“2”);1中的空间利用率为68%.
1 183K以下纯铁晶体的基本结构单元如图1所示,1 183K以上转变为图2所示结构的基本结构单元,在1中铁原子的配位数为8;其中为密堆积的是2(填“1”或“2”);1中的空间利用率为68%.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ②③ | C. | ④⑤ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:3 | B. | 1:2 | C. | 3:4 | D. | 4:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
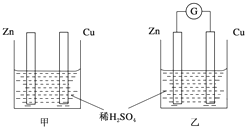 ①分别按图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计.请回答下列问题:
①分别按图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:推断题
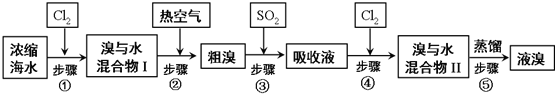
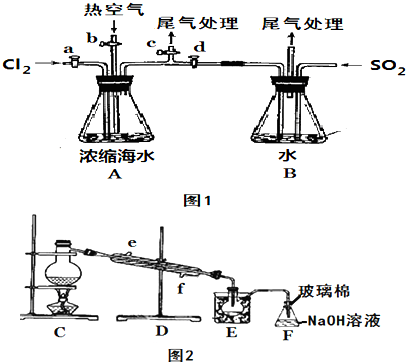
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com