
|
在氯化铁、氯化铜和盐酸混合溶液中加入铁粉,反应结束后,剩余固体滤出后能被磁铁吸引,则反应后溶液中存在较多的阳离子是 | |
A. |
Cu2+ |
B. |
Fe3+ |
C. |
Fe2+ |
D. |
H+ |
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
| A | B |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| 实验编号 | 氨水物质的量浓度 (mol?L-1) |
盐酸物质的量浓度 (mol?L-1) |
混合溶液pH |
| ① | 0.1 | 0.1 | pH=5 |
| ② | C | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH>7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某校化学研究性学习小组欲设计实验验证Al、Fe、Cu的金属活动性,他们提出了以下两种方案.请你帮助他们完成有关实验项目:
某校化学研究性学习小组欲设计实验验证Al、Fe、Cu的金属活动性,他们提出了以下两种方案.请你帮助他们完成有关实验项目:查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

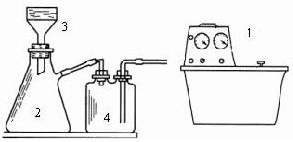
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)已知金属镁与氯化铁和氯化铜溶液反应有多种实验假设。甲、乙两位同学分别设计合理实验步骤探究该反应的历程。
提出猜想:
甲:推测镁与氯化铁、氯化铜水解产生中的H+反应,拉动水解平衡生成生成H2。
乙:推测镁应与氯化铁、氯化铜发生氧化还原反应。
结合对试剂的选择两位同学做了如下实验:
实验过程
编号 | 实验操作 | 预期现象和结论 |
① | 将打磨过的镁条取加入经盐酸酸化的饱和氯化铁溶液,充分反应 | 始终有大量气泡,颜色无明显变化,未见沉淀生成反应完全后取出镁条发现可被磁铁吸引 |
② | 将打磨过的镁条取加入0.1mol/L氯化铁溶液,充分反应 | 有少量气泡,颜色变浅,有红褐色沉淀生成,反应完全后取出镁条发现不能被磁铁吸引 |
根据实验操作,实验现象,甲、乙分别推测解释相应的结论。
(1)写出生成Fe(OH)3胶体的离子方程式:
(2)与甲同学的推测不尽符合的现象是 ,
在实验①③的基础上甲进一步提出猜测:镁与H+反应拉动饱和氯化铁的水解平衡生成Fe(OH)3胶体,故未看到沉淀现象。
要验证甲的进一步猜想,还须补做的实验是
提出你的猜想
(3)乙:根据实验②可推测
(4)结合甲,乙两位同学的推测,你能否谈谈对上述实验事实的认识:
![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com