
����Ŀ����ѧ����һ���������¿���ת��Ϊ���ܣ�
��1����������������Ӧ��
��2FeBr2+3Cl2=2FeCl3+2Br2 ��Na2CO3+2HCl=2NaCl+H2O+CO2��
����������Ӧ�ı����жϣ�����Ϊ������Ƴ�ԭ��ص������Ӧ��ţ��������� ��
��2�������Fe+CuSO4=FeSO4+Cu��Ӧ��ѡ�����˵IJ��Ϻ��Լ����һ��ԭ���
����ԭ���װ��ͼ������ͼ�б�ע���缫�͵������Һ�����ƣ�
��3��д����ԭ��ص缫��Ӧʽ���������������� ��
���𰸡�
��1���٣���Ӧ����������ԭ��Ӧ���е���ת��
��2��

��3��Cu2++2e��=Cu��Zn��2e��=Zn2+
���������⣺��1��ԭ����ǽ���ѧ��ת��Ϊ���ܵ�װ�ã�ֻ��������ԭ��Ӧ���е��ӵ�ת�ƣ�����Ϊ������ԭ��Ӧ������Ƴ�ԭ��أ���Ϊ��������ԭ��Ӧ����������Ƴ�ԭ��أ����Դ��ǣ��٣���Ϊ������ԭ��Ӧ��������Ƴ�ԭ��أ�
��2�������Է���������ԭ��Ӧ������пʧ���ӣ�Ϊ���������������û����Խϲ�Ľ���ͭ����Һ�е�ͭ���ӵõ��ӣ������ÿ��ܵ�ͭ��������ʣ����ԭ��صĹ���������װ��Ϊ��  �����Դ��ǣ�
�����Դ��ǣ�  ��
��
��3��������ʧȥ���ӵļ�������Ҫ���������ã�����CuΪ�����������ǵ�����е������ӷ����õ��ӵĻ�ԭ��Ӧ����Cu2+2e��=Cu������Ϊп������пʧ��������п���ӣ���Zn��2e��=Zn2+�����Դ��ǣ�Cu2+2e��=Cu��Zn��2e��=Zn2+ ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�ij��Һ����ˮ���������H+��OH�����ʵ���Ũ�ȵij˻�Ϊ10��24���ڸ���Һ�У�һ�����ܴ������ڵ������ǣ� ��
A.SO32��B.HCO3��C.NH4+D.NO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������RO3n-�У�����x��������ӣ�Rԭ�ӵ�������ΪA����Rԭ�Ӻ��ں��е�������Ŀ��
A. A-X+n+48 B. A+x-n-24 C. A-x-n-24 D. A-X+n+24
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������뱽�״���ͬ���е�������(����)
A. ����NaOH��Һ��Ӧ B. �����Ʒ�Ӧ�ų�H2
C. ���������� D. ��FeCl3��Һ��Ӧ����ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪H��H��H��O��OO���ļ��ֱܷ�Ϊ436 kJ��mol-1��463 kJ��mol-1��495 kJ��mol-1,�����Ȼ�ѧ����ʽ��ȷ������ ��
A. H2O(g)H2(g)+ ![]() O2(g) ��H=-485 kJ��mol-1
O2(g) ��H=-485 kJ��mol-1
B. H2O(g)H2(g)+ ![]() O2(g)����H=-242.5 kJ��mol-1
O2(g)����H=-242.5 kJ��mol-1
C. 2H2(g)+O2(g)2H2O(g)����H=+485 kJ��mol-1
D. 2H2(g)+O2(g)2H2O(g)����H=-485 kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС�鰴����ʵ����̣��̶������ȼ�ʢ�������ԣ�֤���˺����д��ڵ�Ԫ�أ�
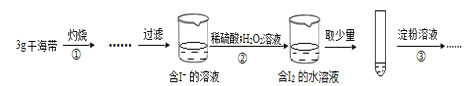
����˵������ȷ����
A. �������Ҫ���ɺ�����������������
B. ����ڷ�Ӧ�����ӷ���ʽΪ��2I- +2H++H2O2 =I2+2H2O
C. ����۲����۲쵽�Թ�����Һ��Ϊ��ɫ������˵�������к��е�Ԫ��
D. ������ڽ��μ�ϡ��������һ���������۲������Թ�����Һ��ɫ�����Ա仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У�����������Ŀ�����ǣ� ��
A. 8g NH3 B. 10g O2 C. 30g Cl2 D. 1g H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һƿ�ס��ҵĻ�����֪���ǵ��������±����ݴˣ����ס��һ���������ѷ�����
���� | �۵� | �е� | �ܶ� | �ܽ��� |
�� | -11.5�� | 198�� | 1.11 gmL-1 | A��B�����Ҿ�������ˮ |
�� | -17.9�� | 290�� | 1.26 gmL-1 |
A. ��ȡ�� B. ���� C. ��Һ�� D. �ᾧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����(����)
A.���ۺ���֬������Ȼ�߷��ӻ�����
B.���Ҵ���ȥ����ϩ����ϩ��ˮ��Ӧ���Ҵ�����ͬһ��Ӧ����
C.��������ˮ�����Ҵ���������Ҵ���������������ͬһ��Ӧ����
D.ʯ�ͷ���õ���ϩ����ϩ������ϩ���л���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com