
【题目】已知Ba的活动性处于Na、K之间,则下列说法中正确的是( )
A. Ba可从KC1溶液中置换出钾B. Ba不能从冷水中置换出氢
C. 在溶液中Zn可还原Ba2+生成BaD. Ba(OH)2是强碱
科目:高中化学 来源: 题型:
【题目】下列叙述相符的是( ) 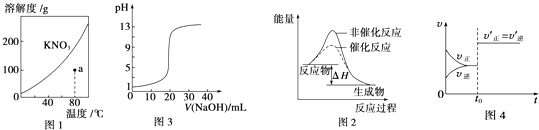
A.图1表示KNO3的溶解度曲线,图中a点对应的溶液是80℃时KNO3的饱和溶液
B.图2表示某吸热热反应分别在有、无催化剂的情况下反应过程中的能量变化
C.图3表示0.1000 molL﹣1 NaOH溶液滴定20.00 mL 0.1000 molL﹣1醋酸溶液的滴定曲线
D.图4表示t0时改变的条件可能是增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳和氨是重要的化工产品,是纯碱工业、制造硝酸、铵盐和氮肥等的原料.
(1)CO2的电子式是 .
(2)以NH3与CO2为原料合成尿素[化学式为CO(NH2)2]的主要反应如下:
①2NH3(g)+CO2(g)═NH2CO2NH4(s)△H=﹣l59.5kJmol﹣1
②NH2CO2NH4(s)CO(NH2)2(s)+H2O(g)△H=+116.5kJmol﹣1
③H2O(1)═H2O(g)△H=+44.0kJmol﹣1
写出CO2与NH3合成尿素和液态水的热化学反应方程式;
(3)NH3和O2在铂系催化剂作用下从145℃就开始反应:4NH3(g)+5O2(g)4NO(g)+6H2O(g)△H=﹣905kJmol﹣1不同温度下NO产率如下图1所示,由此图可知温度对NO产率的影响规律为 , 请用化学反应速率和化学平衡理论解释其原因: . 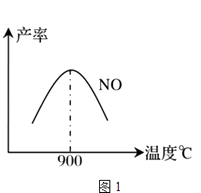
(4)以NO2、O2、熔融NaNO3组成的燃料电池装置如图2所示,在使用过程中石墨I电极反应生成一种氧化物Y,有关石墨I电极反应可表示为 . 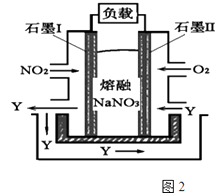
(5)已知常温下NH3H2O的电离平衡常数K=1.75×10﹣5 , H2CO3的电离平衡常数K1=4.4×10﹣7 , K2=4.7×10﹣11 . 常温下,用氨水吸收CO2可得到NH4HCO3溶液,NH4HCO3溶液显(填“酸性”、“中性”或“碱性”);计算反应NH4++HCO3﹣+H2ONH3H2O+H2CO3的平衡常数K=(结果保留2位有效数字).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO是生产羰基化学品的基本原料,对于以水煤气为原料提取CO的工艺,如果氢气
未能充分利用,则提高了CO生产成本,所以在煤化工中常需研究不同温度下的平衡常数、投料比及热值问题.反应CO(g)+H2O (g)H2(g)+CO2(g)的平衡常数随温度的变化如表:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | a |
(1)上述反应的逆反应是(填“放热”或“吸热”)反应.
(2)已知在一定温度下:C(s)+CO2(g)2CO(g) K
C(s)+H2O (g)H2(g)+CO(g) K1
CO(g)+H2O (g)H2(g)+CO2(g) K2
则K、K1、K2、之间的关系是 .
(3)800℃时,在2L的恒容密闭容器中,充入2.0molCO(g)和3.0molH2O(g),保持温度不变进行反应:CO(g)+H2O (g)H2(g)+CO2(g),4min时反应达到平衡,测得CO的转化率为60%.
①0~4min内,CO2的平均反应速率为molL﹣1min﹣1 , 800℃时a= .
②800℃时四个不同容器中发生上述反应,测得各物质的浓度(molL﹣1)如表,其中达到平衡状态的是(填字母).
A | B | C | D | |
c(CO2) | 3 | 1 | 0.8 | 1 |
c(H2) | 2 | 1 | 0.8 | 1 |
c(CO) | 1 | 2 | 3 | 0.5 |
c(H2O) | 2 | 2 | 3 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列填空:
(1)已知在标准状况下的四种气体 ①8.96L CH4②3.01×1022个HCl分子 ③10.2克H2S④0.5molNH3用相应的序号填写下列空白:
体积最大的是;含氢原子数最多的是 .
(2)等物质的量的氧气与臭氧质量之比为 , 分子个数之比为 , 电子个数之比为 .
(3)某金属氯化物MCl3 26.7g,含有0.600mol Cl﹣ . 则金属M的摩尔质量为 .
(4)现有10克H218O中,中子数目为 .
(5)0.4mol NH3中所含氢原子数与g水所含氢原子数相等.
(6)0.5molSO2的质量是g,在标准状况下的体积为L;含有个氧原子.
(7)将标况下22.4L的HCl 溶于水配成200mL的溶液,所溶液的物质的量浓度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用物质的量浓度为18molL﹣1的浓H2SO4来配制450mL0.3mol/L的稀H2SO4 .
可选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒⑥容量瓶 ⑦托盘天平⑧药匙.
请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用到的有(填代号).
(2)经计算,需浓H2SO4的体积为 . 现有①10mL ②50mL ③100mL三种规格的量筒,应选用的量筒是(填代号).
(3)将浓H2SO4加适量蒸馏水稀释,冷却到室温,随后全部转移到 mL的容量瓶中,转移时应用玻璃棒引流.转移完毕,用少量蒸馏水洗涤2~3次,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀.然后缓缓地把蒸馏水直接注入容量瓶直到液面接近刻度1~2cm处.改用加蒸馏水到瓶颈刻度的地方,使溶液的凹面恰好与刻度相切.振荡、摇匀后,装瓶、贴签.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铝热剂冶炼难熔金属,是因为铝( )
①具有导电性 ②具有较强的还原性 ③具有延展性 ④被氧化过程中放出大量的热。
A. ①B. ①②③C. ②④D. ①②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com