
| A. | 该溶液一定呈酸性 | B. | 该溶液中的c(H+)可能等于10-3 | ||
| C. | 该溶液的pH可能为2,可能为12 | D. | 该溶液有可能呈中性 |
分析 由水电离产生的c(OH-)为10-11mol/L,说明该溶液抑制水的电离,可能是酸或碱,pH可能约为11或3,依此进行判断即可.
解答 解:由水电离产生的c(OH-) 为10-12mol/L,说明该溶液抑制水的电离,可能是酸或碱,pH可能约为12或2,
A、该溶液可能是酸或碱,故A错误;
B、该溶液中的c(H+)可能等于10-2mol/L,故B错误;
C、由水电离产生的c(OH-) 为10-12mol/L,说明该溶液抑制水的电离,可能是酸或碱,pH可能约为12或2,故C正确;
D、该溶液可能是酸或碱,不能呈中性,故D错误,
故选C.
点评 本题考查水的电离的影响因素,题目难度不大.要注意酸碱抑制水的电离,掌握基础是解题关键.


 培优三好生系列答案
培优三好生系列答案科目:高中化学 来源: 题型:解答题
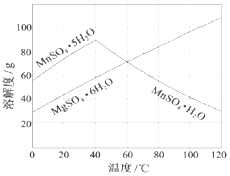 软锰矿(主要成分MnO2,杂质金属元素Fe、Al、Mg等)的水悬浊液与烟气中SO2反应可制备MnSO4•H2O,反应的化学方程式为:MnO2+SO2=MnSO4
软锰矿(主要成分MnO2,杂质金属元素Fe、Al、Mg等)的水悬浊液与烟气中SO2反应可制备MnSO4•H2O,反应的化学方程式为:MnO2+SO2=MnSO4查看答案和解析>>
科目:高中化学 来源: 题型:解答题
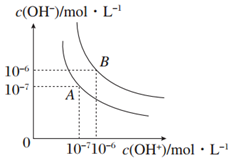 回答下列问题
回答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol•L-1的NaCl溶液是指由1mol NaCl和1000mL水配制成的溶液 | |
| B. | 从1L 0.5mol•L-1的NaCl溶液中取出100mL,剩余溶液物质的量浓度为0.45mol•L-1 | |
| C. | 标准状况下,18克H2O所含的氧原子数目为NA | |
| D. | 0℃时,2mol Cl2的体积不可能为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫氰酸钾溶液 | B. | NaOH溶液 | ||
| C. | 新制氯水、硫氰酸钾溶液 | D. | 酸性KMnO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
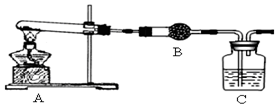
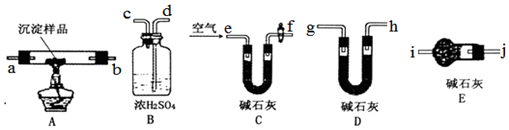
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单阳离子的氧化性:Y>X | |
| B. | 气态氢化物的沸点:Z>M | |
| C. | X、Z与M不可能存在同一离子化合物中 | |
| D. | Y2Z的溶液:c(Y+):c(Z2-)>2:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com