
| A. | 100毫升的溶液中含有Mg2+、Cl-总数为0.3NA | |
| B. | 100毫升的溶液中含有Mg2+数目是0.1NA | |
| C. | 1升溶液中Mg2+的浓度是0.3mol/L | |
| D. | 1.5升溶液中含有Cl-的浓度是4.5mol/L |
分析 A.根据m=cV计算出100mL该溶液中含有氯化镁的物质的量,然后可计算出含有的镁离子、氯离子的说明;
B.根据氯化镁的物质的量计算出含有镁离子的物质的量及数目;
C.镁离子的浓度取决于氯化镁的浓度,与溶液体积大小无关;
D.氯离子的物质的量浓度与溶液体积大小无关,与氯化镁的浓度有关.
解答 解:A.100mL 0.3mol/L的MgCl2溶液中含有氯化镁的物质的量为:0.3mol/L×0.1L=0.03mol,0.03mol氯化镁中含有0.03mol镁离子、0.06mol氯离子,总共含有镁离子、氯离子的总物质的量为0.09mol,含有Mg2+、Cl-总数为0.09NA,故A错误;
B.100mL 0.3mol/L的MgCl2溶液中含有氯化镁的物质的量为0.03mol,0.03mol氯化镁中含有0.03mol镁离子,含有Mg2+数目是0.03NA,故B错误;
C.0.3mol/L的MgCl2溶液中镁离子浓度为0.3mol/L,故C正确;
D.0.3mol/L的MgCl2溶液中氯离子的浓度为:0.3mol/L×2=0.6mol/L,故D错误;
故选C.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的量浓度的概念及表达式为解答关键,注意掌离子的浓度与溶液体积大小无关,为易错点,试题培养了学生的化学计算能力.


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:实验题
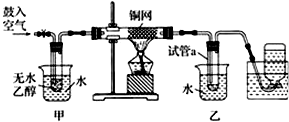
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜片作正极 | B. | 正极反应为:2H++2e-═H2↑ | ||
| C. | 溶液中的H+移向正极 | D. | 锌片作负极,锌发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
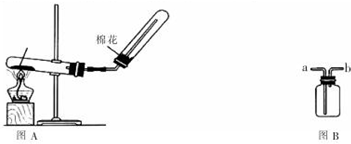
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
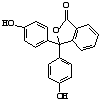
| A. | 分子式为C20H14O4 | |
| B. | 可以发生取代反应、加成反应、氧化反应 | |
| C. | 含有的官能团有羟基、酯基 | |
| D. | 1 mol该物质可与H2和溴水发生反应,消耗H2和Br2的最大值分别为10 mol 和4 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
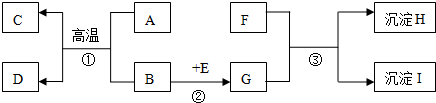
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海水含镁,将金属钠放入海水中可以制取金属镁 | |
| B. | 从海水中提取溴的过程涉及氧化还原反应 | |
| C. | 利用海水制取精盐不涉及化学反应 | |
| D. | 海底多金属结核矿含有Fe、Mn、Co、B等金属 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com