
【题目】在下列变化中,需要加入合适的氧化剂才能实现的是
A.HCl→H2B.CO2→COC.Br-→Br2D.Fe2O3→Fe
科目:高中化学 来源: 题型:
【题目】反应A(g)+3B(g) ![]() 2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是( )
2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是( )
A. v (A)=12 mol / (L·min) B. v (D)=0.4 mol / (L·s)
C. v (C)=30 mol / (L·min) D. v (B)=0.6 mol / (L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置进行实验,甲乙两池均为1 mol·L–1的AgNO3溶液,A、B均为Ag电极。实验开始先闭合K1,断开K2。一段时间后,断开K1,闭合K2,形成浓差电池,灵敏电流计指针发生偏转(提示:Ag+ 浓度越大,氧化性越强)。下列说法不正确的是( )

A. 闭合K1,断开K2后,A电极增重
B. 闭合K1,断开K2后,乙池溶液中Ag+浓度增大
C. 断开K1,闭合K2后,NO3–向A电极移动
D. 断开K1,闭合K2后,B电极发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磁性纳米四氧化三铁在催化剂、DNA检测、疾病的诊断和治疗等领域应用广泛,其制备方法有多种,“共沉淀法”制备纳米Fe3O4的流程如下:

(1)Ⅱ中的反应温度需控制在50℃~60℃之间,实验室控制该温度的最佳方法是___________。
(2)Ⅱ中生成Fe3O4的离子方程式是_____________________________________。
(3)操作Ⅲ包含的方法有_______________。
(4)检验纳米Fe3O4中含有+2价铁元素的方法是_________________________________。
(5)某同学依据上述“共沉淀法”的思路在实验室模拟制备纳米Fe3O4:
① 制备时该同学选择n(Fe3+)∶n(Fe2+)小于2∶1,原因是_______________________。
②经过多次实验发现,当混合溶液中n(Fe3+)∶n(Fe2+)=1∶1时,容易得到理想的纳米Fe3O4。该实验室无FeCl2溶液,现用5mLFeCl3溶液制备Fe3O4,配制n(Fe3+)∶n(Fe2+)=1∶1混合溶液的方法是_____________________(其它试剂和仪器自选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项说法正确的是( )
A.白磷应放在冷水中保存
B.将水注入浓硫酸中以稀释浓硫酸
C.硝酸银放在无色试剂瓶中保存
D.在蒸发皿中加热分解氯酸钾固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)许多金属元素有焰色反应,金属存在焰色反应的原因是___________________________。
(2)基态铝原子中,有______种电子运动状态,其中p轨道的电子云轮廓图的形状为_______。
(3)我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。
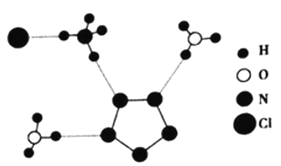
①图中R中阳离子是______(填写化学式),相对分子质量较大的阳离子中心原子的杂化类型是____。
②图中R中阴离子N5-中的σ键总数为___________个。分子中的大π键可用符号![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为![]() ),则N5- 中的大π键应表示为___________。
),则N5- 中的大π键应表示为___________。
(4)氮与铝之间形成化合物X,具有耐高温抗冲击等性能。X的晶体结构如图所示。
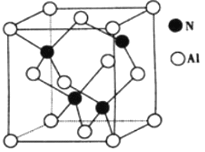
①已知氮化硼与X晶体类型相同,推测氮化硼的熔点比X的熔点___________(填“高”、“低“ ) ,可能的原因是_________________________________________。
②若X的密度为ρg·cm-3,则晶体中最近的两个Al原子的距离为___________cm。(阿伏加德罗常数的值用NA表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组为认识铁及其化合物的性质、分散系的性质做了如下一组综合实验,根据实验流程回答相关问题:

(1)请写出Fe2O3与①反应的离子方程式______________________________。
(2)物质②为_______________。
(3)请写出FeCl3与铁粉反应的化学方程式________________________。
(4)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为____________ ,此过程中发生的氧化还原反应为(用化学方程式表达)_________________________。
(5)将FeCl3饱和溶液滴入沸水中,并继续煮沸至红褐色,制得分散系③为__________________,它与FeCl3溶液、Fe(OH)3浊液的本质区别是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废液是用稀硝酸腐蚀锌板后得到的 ,某化学兴趣小组拟用该废液(含有少量的 Cl-、Fe3+)制取 Zn(NO3)2·6H2O 的过程如下:
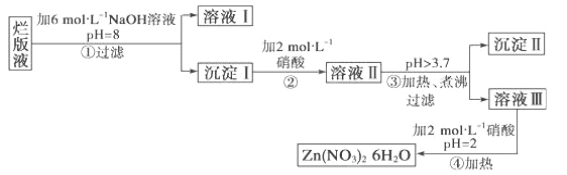
已知:Zn(NO3)2·6H2O 是一种无色晶体,水溶液呈酸性,Zn(NO3)2 能与碱反应,得到的产物 Zn(OH)2 具有
两性,Fe3+在 PH=3.7 时就能完全沉淀。
(1)该废液溶质的主要成分是______(填化学式)。
(2)在操作①中保持 pH=8 的目的是__________________________________________。
(3)沉淀Ⅰ的成分是________________________________________。
(4)操作③中加热、煮沸的目的是______________________________________;
(5)操作④保持 pH=2 的目的是_________________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】装置a、b、c中分别盛有试剂1、2、3,用如图所示的装置进行实验(夹持仪器略去,必要时可加热),能达到相应实验目的的是
选项 | 试剂1 | 试剂2 | 试剂3 | 实验目的 | 装置 |
A | 浓 | Cu片 | KI-淀粉溶液 | 验证 |
|
B | 盐酸 | 石灰石 | 饱和 | 制备 | |
C | 稀硫酸 | 溶液X | 澄清石灰水 | 验证溶液X中是否有 | |
D | 70%硫酸 |
| 酸性 | 证明 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com