
模型法是化学中把微观问题宏观化的最常见方法,对于2HBr(g)⇌H2(g)+Br2(g)反应.下列四个图中可以表示该反应在一定条件下为可逆反应的是()
A.  B.
B.  C.
C.  D.
D. 
科目:高中化学 来源: 题型:
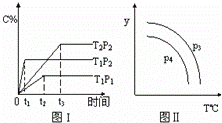
在某容积可变的密闭容器中,有下列的可逆反应:A(g)+B(g)⇌xC(g),有图1(T表示温度,P表示压强,C%表示C的体积分数)所示的反应曲线.若试判断对图2的说法中正确的是( )
|
| A. | P3>P4,y轴表示C的体积分数 |
|
| B. | P3<P4,y轴表示B的质量分数 |
|
| C. | P3<P4,y轴表示混合气体的密度 |
|
| D. | P3>P4,y轴表示混合气体的平均摩尔质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
把VL含有MgSO4和K2SO4的混合溶液分成两份,一份加入a mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡;另一份加入含b mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁.则原混合溶液中钾离子的浓度为()mol/L.
A. 2b﹣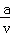 B. 2a﹣
B. 2a﹣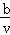 C.
C. 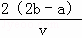 D.
D. 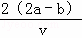
查看答案和解析>>
科目:高中化学 来源: 题型:
电解100mL含c(H+)=0.30mol/L的下列溶液,当电路中通过0.04mol电子时,理论上析出金属质量最大的是()
A. 0.10 mol/L Ag+ B. 0.20 mol/L Zn2+
C. 0.20 mol/L Cu2+ D. 0.20 mol/L Pb2+
查看答案和解析>>
科目:高中化学 来源: 题型:
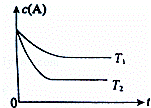
反应A(g)⇌B(g)+C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L.温度T1和T2下A的浓度与时间关系如右图所示.回答下列问题:
(1)上述反应的温度T1小于 T2,平衡常数K(T1) K(T2).(填“大于”、“小于”或“等于”)
(2)若温度T2时,5min后反应达到平衡,A的转化率为70%,则:
①平衡时体系总的物质的量为 .
②反应的平衡常数K= .
③反应在0~5min区间的平均反应速率v(A)= .
查看答案和解析>>
科目:高中化学 来源: 题型:
反应 A+B→C 的反应速率方程式为:v=k c(A)•c(B),v为反应速率,k为速率常数.当c(A)=c(B)=1mol/L时,反应速率在数值上等于速率常数.下列说法正确的是()
A. 只增大c(A)时,v也增大 B. 只增大c(A)时,v值不变
C. 只升高温度时,k值不变 D. 只升高温度时,k值变小
查看答案和解析>>
科目:高中化学 来源: 题型:
电浮选凝聚法处理酸性污水的工作原理如图所示.下列说法不正确的是()
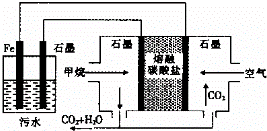
A. 铁电极的电极反应式为:Fe﹣2e﹣═Fe2+
B. 通人空气的石墨电极的电极反应式为O2+2CO2+4e﹣═2CO32﹣
C. 若左池石墨电极产生44.8L(标准状况)气体,则消耗氧气0.5mol
D. 为增强污水的导电能力,可向污水中加入适量工业用食盐
查看答案和解析>>
科目:高中化学 来源: 题型:
用石墨电极电解足量M(NO3)x的水溶液,当阴极上增重a g时,在阳极上同时产生b L氧气(标准状况),从而可知M的相对原子质量为()
A. 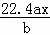 B.
B.  C.
C. 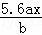 D.
D. 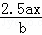
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com