
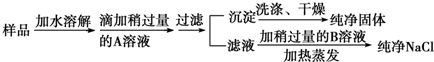
分析 根据粗盐中,所含杂质是CaCl2,故应加入的除杂试剂A为过量的Na2CO3,过滤,所得沉淀为CaCO3,所得滤液中含Na+、Cl-和过量的CO32-,故应加入过量的HCl除去CO32-,所以B为HCl溶液,由于盐酸易挥发,故蒸发结晶即可得纯净的NaCl,据此分析.
解答 解:(1)根据上面的分析可知,加入的A是Na2CO3,发生的反应的化学方程式为Na2CO3+CaCl2=CaCO3↓+NaCl,
故答案为:Na2CO3;Na2CO3+CaCl2=CaCO3↓+NaCl;
(2)根据上面的分析可知,加入的B为HCl,目的是为了除去前面过量的CO32-,反应的化学方程式为Na2CO3+2HCl=CaCl2+CO2↑+H2O,
故答案为:HCl;除去溶液中过量的CO32-;Na2CO3+2HCl=CaCl2+CO2↑+H2O;
(3)由于沉淀CaCO3是从NaCl溶液中过滤出来的,故沉淀上有Cl-和Na+残留,检查CaCO3是否洗净即检查洗涤液中是否有Cl-,即向最后一次洗涤液中加入硝酸酸化的AgNO3溶液,故答案为:硝酸酸化的AgNO3溶液.
点评 本题考查了粗盐的提纯,应注意的是除杂试剂的选择和杂质离子的检验,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ①④②⑤③ | B. | ④①②⑤③ | C. | ②⑤④①③ | D. | ④⑤②①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
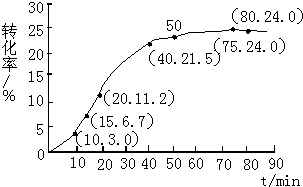 甲酸甲酯水解反应方程式为:
甲酸甲酯水解反应方程式为:| 组分 | HCOOCH3 | H2O | HCOOH | CH3OH |
| 物质的量/mol | 1.00 | 1.99 | 0.01 | 0.52 |
| 反应时间范围/min | 0~5 | 10~15 | 20~25 | 30~35 | 40~45 | 50~55 | 75~80 |
| 平均反应速率/(10-3mol•min-1) | 1.9 | 7.4 | 7.8 | 4.4 | 1.6 | 0.8 | 0.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
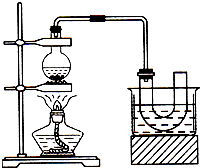 实验室制备溴乙烷(C2H5Br)的装置和步骤如图(已知溴乙烷的沸点38.4℃):
实验室制备溴乙烷(C2H5Br)的装置和步骤如图(已知溴乙烷的沸点38.4℃):查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 如图为实验室制备乙烯的装置图,请回答:
如图为实验室制备乙烯的装置图,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
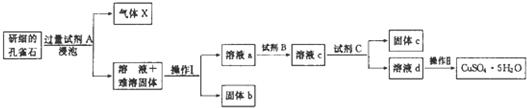
| 物质 | Fe(OH)3 | Cu(OH)2 |
| 开始沉淀时的pH | 2.3 | 4.8 |
| 完全沉淀时的pH | 3.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
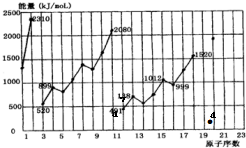 硒是人体必需的微量元素,它在元素周期表中的位置如图所示.
硒是人体必需的微量元素,它在元素周期表中的位置如图所示.| 磷 | 硫 | ||
| 砷 | 硒 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
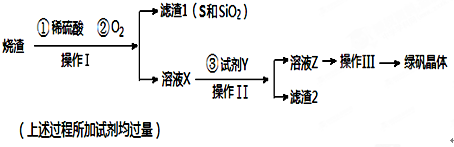
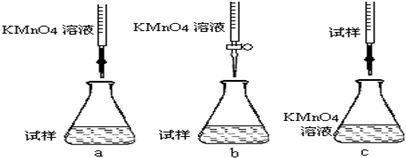
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com