
根据热化学方程式:S(s)+O2(g) SO2(g) ΔH=a kJ·mol-1(a=-297.2)。分析下列说法,其中不正确的是( )
SO2(g) ΔH=a kJ·mol-1(a=-297.2)。分析下列说法,其中不正确的是( )
A.S(s)在O2(g)中燃烧的反应是放热反应
B.S(g)+O2(g) SO2(g) ΔH=b kJ·mol-1,则a>b
SO2(g) ΔH=b kJ·mol-1,则a>b
C.1 mol SO2(g)所具有的能量低于1 mol S(s)与1 mol O2(g)所具有的能量之和
D.16 g固体硫在空气中充分燃烧,可吸收148.6 kJ的热量
科目:高中化学 来源:2015届内蒙古赤峰市元宝山区高二上学期期末化学试卷(解析版) 题型:选择题
下列有关中和热的说法正确的是( )
A.表示中和热的热化学方程式:H+(l)+OH-(l)=H2O(l) ΔH=-57.3 kJ/mol
B.准确测量中和热的实验过程中,至少需测定温度4次
C.中和热的实验过程中,环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小
D.已知2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) ΔH=-114.6 kJ/mol,则该反应的中和热为114.6 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2015届云南省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列实验过程中,始终无明显现象的是( )
A.NO2通入FeSO4溶液中 B.CO2通入CaCl2溶液中
C.NH3通入AlCl3溶液中 D.SO2通入已酸化的Ba( NO3 )2溶液中
查看答案和解析>>
科目:高中化学 来源:2015届云南省云龙县高二下学期期末考试化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.向水中通入氯气:Cl2+H2O=2H++Cl-+ClO-
B.向氯化铁溶液中加入铜:2Fe3++3Cu=2Fe+3Cu2+
C.将含等物质的量的NaHCO3和Ba(OH)2溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O
D.镁和稀硝酸反应:Mg+2H+= Mg2++H2↑
查看答案和解析>>
科目:高中化学 来源:2015届云南省云龙县高二下学期期末考试化学试卷(解析版) 题型:选择题
有机物X、Y、M(M为乙酸)的转化关系为: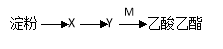 ,下列说法错误的是
,下列说法错误的是
A.X可用新制的氢氧化铜检验
B.反应X→Y中,1molX可生成3molY
C.由Y生成乙酸乙酯的反应属于取代反应
D.可用碘的四氯化碳溶液检验淀粉是否水解完全
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步(人教选修4)1.1.1化学反应与能量的变化(解析版) 题型:选择题
下列各组热化学方程式中,化学反应的ΔH前者大于后者的是( )
①C(s)+O2(g) CO2(g) ΔH1
CO2(g) ΔH1
C(s)+O2(g) CO(g) ΔH2
CO(g) ΔH2
②S(s)+O2(g) SO2(g) ΔH3
SO2(g) ΔH3
S(g)+O2(g) SO2(g) ΔH4
SO2(g) ΔH4
③H2(g)+O2(g) H2O(l) ΔH5
H2O(l) ΔH5
2H2(g)+O2(g) 2H2O(l) ΔH6
2H2O(l) ΔH6
④CaCO3(s) CaO(s)+CO2(g) ΔH7
CaO(s)+CO2(g) ΔH7
CaO(s)+H2O(l) Ca(OH)2(s) ΔH8
Ca(OH)2(s) ΔH8
A.① B.④ C.②③④ D.①②③
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时(人教选修4)4.4金属的电化学腐蚀与防护(解析版) 题型:选择题
钢铁在腐蚀过程中,下列变化可能发生的是( )
①铁元素由+2价转化为+3价
②氧气被还原
③产生氢气
④Fe(OH)3失水生成Fe2O3·xH2O
⑤杂质碳被氧化而除去
A.①②B.③④ C.①②③④ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)第四章检测试卷(解析版) 题型:填空题
有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片与铝片作电极,但甲同学将电极放入6 mol·L-1 H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如图所示。

请回答:
(1)写出甲池中正极的电极反应式: 。
(2)写出乙池中负极的电极反应式和总反应的离子方程式:负极 ,总反应的离子方程式为 。
(3)如果甲、乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出 活动性更强,而乙会判断出 活动性更强(填写元素符号)。
(4)由此实验,可得到如下哪些正确结论? (填写字母序号)。
a.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
b.镁的金属性不一定比铝的金属性强
c.该实验说明金属活动性顺序已过时,已没有实用价值
d.该实验说明化学研究对象复杂,反应受条件影响较大,因此应具体问题具体分析
(5)上述实验也反过来证明了“直接利用金属活动性顺序判断原电池中的正负极”,这种做法 (填“可靠”或“不可靠”)。
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)第一章检测试卷(解析版) 题型:选择题
已知在25 ℃、101 kPa下,1 g C8H18(辛烷)燃烧生成二氧化碳和液态水放出48.40 kJ热量,表示上述反应的热化学方程式正确的是( )
A.C8H18(l)+O2(g) 8CO2(g)+9H2O ΔH=-48.40 kJ·mol-1
8CO2(g)+9H2O ΔH=-48.40 kJ·mol-1
B.C8H18(l)+O2(g) 8CO2(g)+9H2O(l) ΔH=-5 518 kJ·mol-1
8CO2(g)+9H2O(l) ΔH=-5 518 kJ·mol-1
C.C8H18(l)+O2(g) 8CO2(g)+9H2O(l) ΔH=+5 518 kJ·mol-1
8CO2(g)+9H2O(l) ΔH=+5 518 kJ·mol-1
D.C8H18(l)+O2(g) 8CO2(g)+9H2O(l) ΔH=+48.40 kJ·mol-1
8CO2(g)+9H2O(l) ΔH=+48.40 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com