
| A、它们所含的电子数目之比为1:1 |
| B、它们所含的O原子数目之比为1:2 |
| C、它们所含的C原子数目之比为1:1 |
| D、它们所含的原子总数目之比为2:3 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、反应是吸热还是放热须看旧键断裂吸收的能量和新键生成释放的能量的大小 |
| B、需要加热才能进行的反应是吸热反应 |
| C、反应热的大小与反应物所具有的能量和生成物所具有的能量无关 |
| D、伴有能量变化的变化都是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、需要加热才能发生的反应一定是吸热反应 |
| B、放热反应在常温下一定很容易发生 |
| C、吸热反应在一定的条件下也能发生 |
| D、焓变的符号是△H,单位是kJ?mol-1,反应热的单位是kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧的摩尔质量是32g/mol |
| B、Al3+的摩尔质量是27g/mol |
| C、2molCO2的质量是88g/mol |
| D、1molH2S的摩尔质量是34g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由于碘在酒精中的溶解度大,所以可用酒精把碘水中的碘萃取出来 |
| B、水的沸点为100℃,酒精的沸点为78.5℃,所以可用加热蒸馏方法,使含水的酒精变为无水酒精 |
| C、四氯化碳和水混合后,可用分液的方法来分离 |
| D、NaCl溶解度随温度下降而减小,所以用冷却法从热的含少量KNO3的NaCl溶液中分离得到纯净的NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AB |
| B、AB2 |
| C、AB3 |
| D、A2B3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子核外电子排布呈周期性变化 |
| B、元素的相对原子质量逐渐增大 |
| C、原子半径呈现从大到小的周期性变化 |
| D、元素化合价呈周期性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O | ||||
| B、Ba(OH)2溶液中逐滴滴加NaHSO4至中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O | ||||
C、用饱和氯化铁溶液和沸水反应制取氢氧化铁胶体:Fe3++3H2O
| ||||
| D、在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2 Fe(OH)3=2 FeO42-+3Cl-+5H2O+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、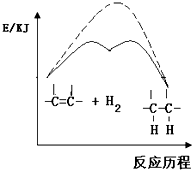 说明烯烃与H2的加成反应是放热反应,虚线表示在有催化剂的条件下表示 |
B、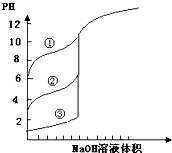 用0.1000mol/L NaOH溶液分别滴定浓度相同的三种一元酸,曲线可确定①的酸性最强 |
C、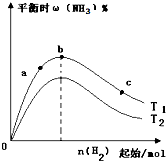 表示合成氨反应在其他条件不变的情况下,改变起始n(H2)对平衡的影响.由此可知,N2转化率最高的是b点;且T1>T2,K2>K1(T1和T2 表示温度,K1、K2表示对应温度下的平衡常数) |
D、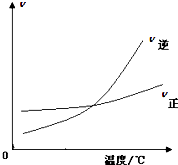 表示可逆反应“A2(g)+3B2 (g)?2AB3(g)”△H小于0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com