
| A. | 酯的一般通式是RCOOR′和R′可以相同,也可以不同 | |
| B. | RCOOR′和R′可以是脂肪烃基,也可以是芳香烃基 | |
| C. | 在RCOOR′中,当R和R′均为-CH3时,这种酯叫甲酸甲酯 | |
| D. | 碳原子数相同的饱和一元羧酸和饱和一元酯互为同分异构体 |
分析 A.根据酯的一般通式是RCOOR′分析;
B.根据R和R′的特点分析;
C.R和R′均为-CH3时,为乙酸甲酯;
D.饱和一元羧酸和饱和一元酯,通式为CnH2nO2,碳原子数相同互为同分异构体.
解答 解:A.酯的一般通式是RCOOR′,R和R′可以相同,也可以不同,故A正确;
B.RCOOR′中,R和R′可以是脂肪烃基,也可以是芳香烃基,故B正确;
C.在RCOOR′中,当R和R′均为-CH3时,这种酯叫乙酸甲酯,故C错误;
D.碳原子数相同的饱和一元羧酸和饱和一元酯,通式为CnH2nO2,互为同分异构体,故D正确;
故选C.
点评 本题考查了同系物的判断,题目难度不大,注意掌握同系物的概念及判断方法,明确具有相同的通式的有机物不一定互为同系物,但是同系物一定具有相似结构、相同通式.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:选择题
| A. | H2D与H2T互为同素异形体 | |
| B. | 不同元素的原子构成的分子只含极性共价键 | |
| C. | ${\;}_{92}^{235}$U和${\;}_{92}^{238}$U是中子数不同、质子数相同的同种核素 | |
| D. | 短周期第 IVA与第 VIIA族元素的原子间构成的分子,均满足原子最外层8电子结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
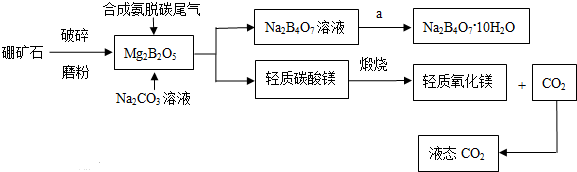
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器 | 起始各物质的物质的量/mol | 达到平衡时体系能量的变化 | |||
| SO2 | O2 | SO3 | Ar | ||
| 甲 | 2 | 1 | 0 | 0 | 放出热量:Q1 |
| 乙 | 1.8 | 0.9 | 0.2 | 0 | 放出热量:Q2=78.8kJ |
| 丙 | 1.8 | 0.9 | 0.2 | 0.1 | 放出热量:Q3 |
| A. | Q1>Q3>Q2=78.8kJ | |
| B. | 三个容器中反应的平衡常数均为K=2 | |
| C. | 甲中反应达到平衡时,若升高温度,则SO2的转化率将大于50% | |
| D. | 若乙容器中的反应经tmin达到平衡,则0~tmin内,v(O2)=$\frac{1}{5t}$ mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | b点时,溶液中微粒浓度大小的关系:c(CN-)>c(Cl-)>c(HCN)>c(OH-)>c(H+) | |
| B. | d点溶液存在的关系:c(Na+)+c(H+)=c(HCN)+c(OH-)+2c(CN-) | |
| C. | 图2中的e点对应图1中的c点 | |
| D. | 在滴定过程中选用酚酞试剂比选用甲基橙试剂作指示剂误差更小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径Z>W>Y>X | |
| B. | 气态氢化物的稳定性Z>W | |
| C. | Y的最高价氧化物对应的水化物可与其气态氢化物发生化合反应 | |
| D. | X的气态氢化物与足量W单质在光照条件下反应所得生成物均为气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol Na2O和Na2O2的混合物中,阴阳离子总数为3NA | |
| B. | 非标准状况下,NA个CO2分子所占的条件不可能为22.4L | |
| C. | 24.4gNa2O•SiO2中含有0.2NA个SiO2分子 | |
| D. | 56gFe投入1000mL3.5mol•L-1稀硝酸中,充分反应,转移电子总数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述气态化合物分子中所有原子最外层电子数均为8 | |
| B. | X、N、Z都可与W形成既有极性共价键又有非极性共价键的化合物 | |
| C. | 化合物W4XY2Z可能是离子化合物,也可能是共价化合物 | |
| D. | 沸点:W2Z>YW3>XW4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com