
写出下列典型物质的电离方程式
(1)H2SO4_________________________________________________________________;
(2)H2CO3_________________________________________________________________;
(3)Ca(OH)2________________________________________________________________;
(4)NH3·H2O_______________________________________________________________;
(5)NaCl___________________________________________________________________;
(6)BaSO4_________________________________________________________________;
(7)NaHSO4________________________________________________________________;
(8)NaHCO3________________________________________________________________;
(9)NaHSO4(熔融)___________________________________________________________;
(10)CH3COOH_____________________________________________________________。
科目:高中化学 来源: 题型:
氢能是最重要的新能源。储氢作为氢能利用的关键技术,是当前关注的热点之一。
⑴氢气是清洁能源,其燃烧产物为 。
⑵NaBH4是一种重要的储氢载体,能与水反应生成NaBO3,且反应前后B的化合价不变,该反应的化学方程式为,反应消耗1molNaBH4时转移的电子数目为。
⑶储氢还可借助有机物,如利用环已烷和苯之间的可逆反应来实现脱氢和加氢。

 (g)
(g)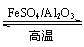


 (g)+3H2(g)
(g)+3H2(g)
在某温度下,向恒容容器中加入环已烷,其起始浓度为amol·L-1,平衡时苯的浓度为bmol·L-1,该反应的平衡常数K=
⑷一定条件下,题11图所示装置可实现有机物的电化学储氢(忽略其它有机物)。


①导线中电子转移方向为 。(用A、D表示)
②生成目标产物的电极反应式为 。
③该储氢装置的电流效率η= 。(η=生成目标产物消耗的电子数/转移的电子总数×100%,计算结果保留小数点后1位。)
查看答案和解析>>
科目:高中化学 来源: 题型:
500 mL 2 mol·L-1 FeCl3溶液和500 mL 2 mol·L-1明矾溶液分别滴入沸水中,加热制成分散系甲、乙,经测定,甲分散系中分散质的粒子直径大小在1~100 nm之间,乙分散系中分散质的粒子直径大小在10-9~10-7 m之间。下列关于甲、乙分散系的判断合理的是
( )
A.在暗室里用一束明亮的“强光”照射甲、乙,发现甲有丁达尔效应,乙没有丁达尔效应
B.向甲、乙中分别滴加过量的氢氧化钠溶液,现象都是“先聚沉,后溶解”
C.向甲、乙中分别滴加过量的氢碘酸,最终现象分别是深褐色溶液、无色溶液
D.蒸干、灼烧FeCl3溶液和明 矾溶液会得到对应的固体盐
矾溶液会得到对应的固体盐
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组的同学们按照下面的实验方法制备氢氧化铁胶体:首先取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和的FeCl3溶液继续煮沸,至液体呈透明的红褐色。
FeCl3+3H2O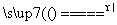 Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl
(1)判断胶体制备是否成功,可利用胶体的____________。
(2)在做制备氢氧化铁胶体的实验时,有些同学没有按要求进行,结果没有观察到胶体,请你预测其现象并分析原因:
①甲同学没有选用饱和氯化铁溶液,而是将稀氯化铁溶液滴入沸水中,结果没有观察到________________,其原因是____________________________________________。
②乙同学在实验中没有使用蒸馏水,而是用自来水,结果会________________________,原因是______________________________________________。
③丙同学向沸水中滴加饱和氯化铁溶液后,长时间加热,结果会___________________,原因是________________________________________。
(3)丁同学按要求制备了Fe(OH)3胶体,但是他又向Fe(OH)3胶体中逐滴加入了稀H2SO4溶液,结果出现了一系列变化。
①先出现红褐色沉淀,原因是_______________________________________________。
②随后沉淀溶解,此反应的离子方程式是_____________________________________
______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
完成下列反应的离子方程式:
(1)Ba(OH)2溶液与(NH4)2SO4溶液混合:____________________________________。
(2)CuSO4溶液与Ba(OH)2溶液混合:_______________________________________。
(3)NH4HCO3与过量NaOH溶液混合:______________________________________。
(4)Ba(OH)2与H2SO4两稀溶液混合:_______________________________________。
(5)Fe2O3溶于HI溶液中:________________________________________________。
(6)FeBr2溶液中通入过量Cl2:____________________________________________。
(7)FeO溶于稀HNO3中:_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示对应化学反应的离子方程式正确的是 ( )
A.MnO2与浓盐酸反应制Cl2:MnO2+4HCl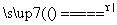 Mn2++2Cl-+Cl2↑+2H2O
Mn2++2Cl-+Cl2↑+2H2O
B.明矾溶于水产生Al(OH)3胶体:Al3++3H2O===Al(OH)3↓+3H+
C.Na2O2溶于水产生O2:Na2O2+H2O===2Na++2OH-+O2↑
D.Ca(HCO3)2溶液与少量NaOH溶液反应:HCO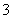 +Ca2++OH-===CaCO3↓+H2O
+Ca2++OH-===CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
由短周期元素组成的化合物X是某抗酸药的有效成分。甲同学欲探究X的组成。
查阅资料:①由短周期元素组成的抗酸药的有效成分有碳酸氢钠、碳酸镁、氢氧化铝、硅酸镁铝、磷酸铝、碱式碳酸镁铝。
②Al3+在pH=5.0时沉淀完全;
Mg2+在pH=8.8时开始沉淀,在pH=11.4时沉淀完全。
实验过程:
Ⅰ.向化合物X粉末中加入过量盐酸,产生气体A,得到无色溶液。
Ⅱ.用铂丝蘸取少量Ⅰ中所得的溶液,在火焰上燃烧,无黄色火焰。
Ⅲ.向Ⅰ中所得的溶液中滴加氨水,调节pH至5~6,产生白色沉淀B,过滤。
Ⅳ.向沉淀B中加过量NaOH溶液,沉淀全部溶解。
Ⅴ.向Ⅲ中得到的滤液中滴加NaOH溶液,调节pH至12,得到白色沉淀C。
(1)Ⅰ中气体A可使澄清石灰水变浑浊,A的化学式是__________。
(2)由Ⅰ、Ⅱ判断X一定不含有的元素是磷、__________。
(3)Ⅲ中生成B的离子方程式是__________。
(4)Ⅳ中B溶解的离子方程式是__________。
(5)沉淀C的化学式是__________。
(6)若上述n(A)∶n(B)∶n(C)=1∶1∶3,则X的化学式是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,是由碳棒、铁片和氯化铜溶液组成的原电池,下列叙述正确的是
 A.碳棒为正极
A.碳棒为正极
B.碳棒上的电极反应式为2H2O + O2 + 4e- = 4OH—
C.铁片上的电极反应式为2Cl——2e- = Cl2↑
D.铁片为阴极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com