
| A、SiCl4、PCl5分子中各原子最外层均达到8电子稳定结构 |
B、右表中的数字代表的是元素的原子序数.表中数字所对应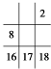 的元素与它们在周期表中的位置是相符的 的元素与它们在周期表中的位置是相符的 |
| C、元素的化学性质主要决定于核外电子数 |
| D、元素周期表中金属和非金属元素分界线附近的元素没有用于制造半导体材料的 |


科目:高中化学 来源: 题型:
| A、溶质仅含NaHCO3 |
| B、c(Na+)=2c(CO32-)+c(HCO3-)+c(H2CO3) |
| C、c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| D、c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用试纸检验气体性质时,可用手拿着试纸,并用蒸馏水将试纸润湿,置于盛有待测气体的试管口附近,观察试纸颜色的变化 |
| B、已知在K2CrO4溶液中存在如下平衡:2CrO42-(黄色)+2H+═Cr2O72-(橙色)+H2O,则向黄色的K2CrO4溶液中,加入几滴浓硫酸,可使溶液颜色转化为橙色 |
| C、用乙醇制取乙烯的实验中,为防止副反应的发生,应用酒精灯加热将混合溶液迅速升温 |
| D、利用银镜反应验证蔗糖是否水解时,应先向蔗糖的水解液中加入氢氧化钠溶液使溶液呈碱性后,再加入新制的银氨溶液并加热,观察现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | Li | Na | K | O | O- | F |
| 电子亲和能/kJ?mol-1 | 59.8 | 52.7 | 48.4 | 141 | -780 | 327.9 |
| A、电子亲和能越大,说明越难得到电子 |
| B、基态的气态氟原子得到一个电子成为氟离子时放出327.9kJ的能量 |
| C、氧元素的第二电子亲和能是-780 kJ?mol-1 |
| D、基态的气态氧原子得到两个电子成为O2-需要吸收能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾[KAl(SO4)2?12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 |
| B、用蒸馏水充分浸润燃尽后的火柴头,然后加入硝酸银和稀硝酸检验火柴头中氯元素 |
| C、浓H2SO4有强氧化性,常温下能与Cu发生剧烈反应 |
| D、用食醋和碘化钾淀粉试纸可以鉴别NaNO2和NaCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com