
| A���ؽᾧ��һ�������ڱ��ᴿ���л������ܼ��е��ܽ�����¶�Ӱ��ϴ�Ļ����ķ��� |
| B�����л�����Ӻ������ͼ���о�������ȷ���л�����Է������� |
| C��ȼ�շ���ȷ���л�����ӹ����ŵ���Ч���� |
| D������ͨ�����ڷ���ȷ���л�����ӵ�Ԫ����� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Na2S��ȥ��ˮ�е�Hg2+��Hg2++S2-�THgS�� |
| B��������Һ����ϴ���ۣ�CO32-+2H2O?H2CO3+2OH- |
| C���������Ȼ���ʱ�������̣�NH3+HCl=NH4Cl |
| D�����ҽ���Һ�м������ᡢ˫��ˮ��2I-+2H++H2O2�TI2+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| A��1mol KClO3�μӷ�Ӧ��������������Ϊ44.8L |
| B��H2C2O4�ڷ�Ӧ�б���ԭ |
| C��ClO2�������������������ˮ���ھ�ˮʱ�������� |
| D������1mol ClO2����Ӧ��ת�Ƶĵ�����1 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����50g��������Ϊ46%���Ҵ�ˮ��Һ�У�������ԭ����Ϊ3NA |
| B��Na2S��Na2O2 ��������15.6g�У����е���������Ϊ0.3NA |
| C��104g����ϩ�к���8NA��̼�����4NA��̼̼˫�� |
| D��1.6g�������ͳ�����ɵĻ�����к�����ԭ�ӵ���ĿΪ0.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| X | Y | |
| W | M | Z |
| A��Mλ��Ԫ�����ڱ��е������ڢ�A�� |
| B��ԭ�Ӱ뾶��Z��M��X |
| C����̬�⻯������ȶ��ԣ�Y��X��W |
| D��W�������������NaOH��Ӧ��Ҳ����HF��Ӧ���������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 Ǧ���仯������������ء������豸��X���߷������ϣ���֪Pb�Ļ��ϼ�ֻ��0��+2��+4�ش��������⣺
Ǧ���仯������������ء������豸��X���߷������ϣ���֪Pb�Ļ��ϼ�ֻ��0��+2��+4�ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 Ԫ��R��X��T��Z��Q��Ԫ�����ڱ��е����λ�����±���ʾ������ֻ��X�Ƕ����ڵĽ���Ԫ�أ������ж���ȷ���ǣ�������
Ԫ��R��X��T��Z��Q��Ԫ�����ڱ��е����λ�����±���ʾ������ֻ��X�Ƕ����ڵĽ���Ԫ�أ������ж���ȷ���ǣ�������| A��X�����������������ǿ�� |
| B���ǽ����ԣ�T��R |
| C����̬�⻯���ȶ��ԣ�T��Z |
| D��R��Q��ԭ�Ӻ�����������16 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
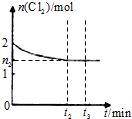 ������COCl2����������N2H4����H2O2������Ҫ�Ĺ�ҵ��ֵ��
������COCl2����������N2H4����H2O2������Ҫ�Ĺ�ҵ��ֵ��| ���� | ��Ӧ�� Ͷ����� | ƽ��ʱ n��Cl2��/mol | �ﵽƽ�� ����ʱ��/min | ƽ��ʱ �����仯/kJ |
| �� | 1mol COCl2 | n1 | t1 | ����Q1 |
| �� | 2mol Cl2��2mol CO | n2 | t2 | ����Q2 |
| �� | 2mol COCl2 | n3 | t3 | ����Q3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com