
| A、甲烷与丁烯 |
| B、甲烷与丙烯 |
| C、丙烷与乙烯 |
| D、乙烷与丙烯 |
| 4.48L |
| 22.4L/mol |


科目:高中化学 来源: 题型:
| A、硅酸铜钡可用氧化物形式表示为BaO?CuO?2SiO2 |
| B、强酸、强碱均可将硅酸铜钡(BaCuSi2O6)完全溶解 |
| C、将CO2通入硅酸钠溶液中,可形成硅酸溶胶 |
| D、泡花碱可以用作防火材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、CO的燃烧热为283 kJ |
B、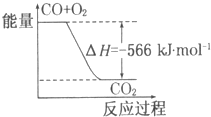 如图可表示由CO生成CO2的反应过程和能量关系 |
| C、2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)△H=-452 kJ/mol |
| D、CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为2x6.02×l023 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 外,还有
外,还有 ,n个
,n个 ,其余为-OH,则-OH的个数为
,其余为-OH,则-OH的个数为查看答案和解析>>
科目:高中化学 来源: 题型:
| 物 质 | CH4 | CO2 | CO | H2 |
| 平衡浓度(mol?L-1) | 0.5 | 1.0 | 1.0 | 1.0 |

| 物质 | Na | S | Al2O3 |
| 熔点/℃ | 97.8 | 115 | 2050 |
| 沸点/℃ | 892 | 444.6 | 2980 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、③ | B、③⑤ | C、①②③ | D、②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②④ | B、①② |
| C、②③⑤ | D、②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com