
| A、6个 | B、10个 |
| C、8个 | D、28个 |
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
| A、单位时间内减少n mol A2,同时生成2n mol AB |
| B、单位时间内生成n mol B2,同时生成n mol AB |
| C、单位时间内生成 2xmol AB,同时生成xmol A2 |
| D、容器内各组成成分的物质的量之和不随时间变化而变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、新制氯水中只含Cl2和H2O分子 |
| B、新制氯水可使蓝色石蕊试纸先变红后褪色 |
| C、光照氯水有气泡逸出,该气体是Cl2 |
| D、氯水放置数天后酸性下降 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由极性键构成的极性分子 |
| B、由极性键构成的非极性分子 |
| C、由非极性键构成的极性分子 |
| D、中心原子采用sp2杂化的分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,等体积的CH4和CO2所含共用电子对数相等 |
| B、与NaOH溶液、H2SO4溶液反应产生等量H2,所需铝粉质量相等 |
| C、1 mol OH-和17 g NH3所含电子数相等 |
| D、明矾溶液中K+和Al3+物质的量浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol H2O的质量为18 g/mol |
| B、CH4的摩尔质量为16 g |
| C、3.01×1023个SO2分子的质量为32 g |
| D、2mol NaOH溶于1 L水中配成溶液的浓度为2 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HD、NaOH都属于化合物 |
| B、碳素钢、不锈钢和目前流通的硬币都属于合金 |
| C、浓盐酸、浓硫酸、浓硝酸都属于氧化性酸 |
| D、氨水、醋酸、氢氧化铝都属于弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
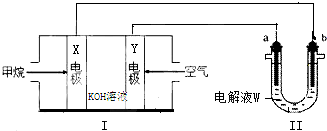
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com