
| A、高温下,0.2mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA | ||||
| B、室温下,1L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA | ||||
| C、氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | ||||
D、5NH4NO3
|
| 8 |
| 3 |
| 1.6 |
| 3 |
| ||
| 2 |
| 4 |
| 15 |
| 4 |
| 15 |
| 15mol |
| 4 |


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
| 浓硫酸 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向苏打和小苏打溶液中分别加入盐酸 | 均冒气泡 | 两者均能与盐酸反应 |
| B | 向AgNO3溶液中滴加过量氨水 | 溶液澄清 | Ag+与NH3?H2O能大量共存 |
| C | 将可调高度的铜丝伸入到稀HNO3中 | 溶液变蓝 | Cu与稀HNO3发生置换反应 |
| D | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置 | 下层溶液显紫红色 | 氧化性:Fe3+>I2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 配料 | 氯化钠(NaCl)、碘酸钾(KIO3) |
| 含碘量 | (35±15)mg?kg-1(以I计) |
| 食用方法 | 菜未烧熟不宜加入加碘盐,菜烧熟后加入加碘盐最佳. |
| A、此食盐是纯净物 |
| B、“菜未烧熟不宜加入加碘盐”的原因可能是碘酸钾受热不稳定 |
| C、“加碘食盐”中的“碘”是指碘单质 |
| D、1kg此食盐中含碘酸钾(35±15)mg |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该溶液中所含的离子是:Fe2+、K+、SO42-、NO3- |
| B、实验③,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为18g |
| C、若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色 |
| D、若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液会显血红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁表面镀锌可增强其抗腐蚀性 |
| B、用聚乙烯塑料代替聚乳酸塑料可减少白色污染 |
| C、大量燃烧化石燃料是造成雾霾天气的一种重要因素 |
| D、含重金属离子的电镀废液不能随意排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、④⑤⑨ | B、⑦⑧⑩ |
| C、①②③⑨ | D、②⑦⑨⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:
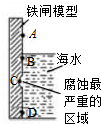 铁及其化合物与生产、生活关系密切.
铁及其化合物与生产、生活关系密切.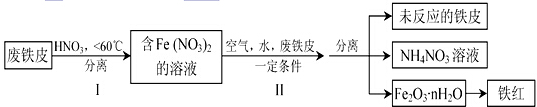
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com