
【题目】一块表面已部分被氧化为氧化钠的金属钠样品5.4g,将其投入94.7g 水中,放出1120mL H2(标准状况下)。
(1)请写出该样品放入水中时发生的反应的化学方程式:_______。滴加酚酞后溶液颜色_______,由此可知溶液呈_______ (“酸性”“碱性” 、 或“中性”)。
(2)样品中含金属钠_______g。
(3)所得的溶液的质量分数为_______。
【答案】 2Na+2H2O=2NaOH+H2↑ Na2O+H2O= 2NaOH 变红 碱性 2.3g 8%
【解析】试题分析:本题考查钠、氧化钠与水的反应,有关混合物和溶质质量分数的计算。
(1)金属钠已部分被氧化为氧化钠,所以样品放入水中发生反应的化学方程式为2Na+2H2O=2NaOH+H2↑、Na2O+H2O=2NaOH。反应后生成的溶液为NaOH溶液,溶液呈碱性,滴加酚酞后溶液变红色。
(2)n(H2)=1.12L![]() 22.4L/mol=0.05mol,根据方程式2Na+2H2O=2NaOH+H2↑,n(Na)=0.1mol,样品中m(Na)=0.1mol
22.4L/mol=0.05mol,根据方程式2Na+2H2O=2NaOH+H2↑,n(Na)=0.1mol,样品中m(Na)=0.1mol![]() 23g/mol=2.3g。
23g/mol=2.3g。
(3)由钠生成的NaOH物质的量为0.1mol;样品中氧化钠的质量m(Na2O)=5.4g-2.3g=3.1g,n(Na2O)=3.1g![]() 62g/mol=0.05mol,根据方程式Na2O+H2O=2NaOH,由氧化钠生成的NaOH物质的量为0.1mol;反应后共生成NaOH物质的量为0.1mol+0.1mol=0.2mol,共生成NaOH的质量为0.2mol
62g/mol=0.05mol,根据方程式Na2O+H2O=2NaOH,由氧化钠生成的NaOH物质的量为0.1mol;反应后共生成NaOH物质的量为0.1mol+0.1mol=0.2mol,共生成NaOH的质量为0.2mol![]() 40g/mol=8g,根据质量守恒定律,反应后溶液的总质量为m(样品)+m(H2O)-m(H2)=5.4g+94.7g-0.05mol
40g/mol=8g,根据质量守恒定律,反应后溶液的总质量为m(样品)+m(H2O)-m(H2)=5.4g+94.7g-0.05mol![]() 2g/mol=100g,则所得溶液中NaOH的质量分数为8g
2g/mol=100g,则所得溶液中NaOH的质量分数为8g![]() 100g
100g![]() 100%=8%。
100%=8%。


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】现有一瓶无色澄清的溶液,可能由以下离子中的几种组成:Na+、K+、NH4+、Fe2+、SO42-、I-、CO32-、Cl-、SO32-、MnO4-,请根据以下实验步骤及现象回答问题:
步骤一:取适量待测液,加入NaOH溶液并加热,得到溶液A,并产生刺激性气味的气体
步骤二:向溶液A加入足量稀盐酸和BaCl2溶液,得到溶液B、白色沉淀和有刺激性气味的气体
步骤三:往B溶液中通入适量Cl2,得到黄褐色溶液C
(1)下列有关该溶液说法正确的是__________。
A. 一定存在SO42-、I-、NH4+、SO32-
B. 一定不存在Fe2+、CO32-、MnO4-
C. 可能存在CO32-、Cl-、Na+、K+
D. 可用AgNO3溶液确认原溶液中是否存在Cl-
(2)步骤三得到黄褐色溶液的离子方程式是____________。
(3)若向原溶液中先加入足量的盐酸,再加入足量的________(填化学式)并加热,通过现象也能得出步骤一、二相同的结论。
(4)对于溶液中还可能存在的阳离子,确认其存在的实验方法是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不导热的恒容密闭容器中通入CO(g)和H2O(g),一定条件下使反应CO(g)+H2O(g) ![]() CO2(g)+H2(g)达到平衡状态,正反应速率随时间变化的示意图如下所示。由图可得出的正确结论是
CO2(g)+H2(g)达到平衡状态,正反应速率随时间变化的示意图如下所示。由图可得出的正确结论是
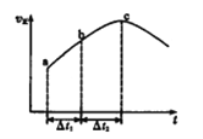
A. 反应物浓度:a点小于c点
B. c点时反应进行的程度最大
C. 该反应的正反应为吸热反应
D. △t1=△t2时,生成H2的物质的量:a~b段小于b~c段
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法正确的是( )
A.厨房中用的食盐、食醋都是电解质
B.95%的医用酒精溶液可用于环境消毒
C.硅胶和生石灰均可用作食品包装袋内的干燥剂
D.石英玻璃、普通玻璃、钢化玻璃都属于硅酸盐产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环已酮是工业上的一种重要有机合成原料和溶剂.实验室制备原理为: ,其反应的装置示意图如下(夹持装置加热装置略去):
,其反应的装置示意图如下(夹持装置加热装置略去):
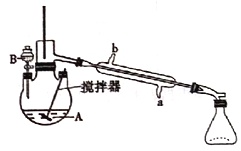
已知:
物质 | 沸点(℃) | 密度(g·cm-3,20℃) | 溶解性 |
环己醇 | 161.1(97.8) | 0.962 | 能溶于水 |
环已酮 | 155.6(95) | 0.948 | 微溶于水 |
(注:括号中的数据表示该有机物与水形成的具有固定组成的恒沸物的沸点)
(1)制备产品。通过仪器B____(填仪器名称)将酸性Na2Cr2O7和H2SO4混合溶被加到盛有环已醇的三颈烧瓶A中,通过______(填序号)方法加热到55-60℃进行反应。
a.酒精灯加热 b.油浴加热 c.水浴加热
(2)分离粗品。反应完成后,加入适量水,蒸馏,收集95-100℃的馏分(主要含环已酮粗品和水的混合物),试解释无法分离环己酮和水的原因是____________。
(3)提纯环已酮。
①在收集到的粗品中加NaCl固体至饱和,静置,分液。加入NaCl固体的作用是________。
②加入无水MgSO4固体,除去有机物中________ (填物质名称)。
③过滤,蒸馏,收集151-156℃馏分,得到精品。
(4)下列关于实验的叙述中,错误的是________。
A.冷凝管的冷水应该从b进从a出
B.实验开始时,温度计水银球应插入反应液中,便于控制反应液的温度
C.装置B中也可加入Na2Cr2O7和稀盐酸混合溶液
D.反应过程中,需不断搅拌
(5)利用环已酮做萃取剂可分离含Co2+、Mn2+的溶液,根据下图信息可判断,将pH范围控制在_______左右时可分离出Mn2+。
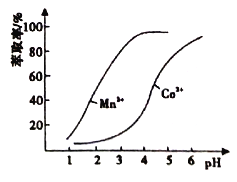
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实,不能用勒夏特列原理解释的是
A. 用排饱和氯化钠溶液的方法来收集氯气
B. 配制和保存硫酸铁溶液常加入适量稀硫酸
C. 向氢氧化镁悬浊液中加入饱和氯化铵溶液,溶液变澄清
D. 对2 HI (g)![]() H2 (g) + I2 (g)的平衡体系,增大压强使颜色变深
H2 (g) + I2 (g)的平衡体系,增大压强使颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物是我们熟悉的典型非金属元素,研究它们的性质对于生产、生活、科研具有重要意义,请回答以下问题:
I.(1)图为制取氨气的装置和选用的试剂,其中错误的是______.(填字母)
A.①② B.②③ C.③④ D.①③

(2)实验室制备氨气的化学反应方程式是_______________________________________为了得到干燥的 NH3,可用_______做干燥剂。若有5.35g氯化铵参加反应,则产生的气体在标准状况下的体积为______L.
II.铵盐受热易分解,如图所示
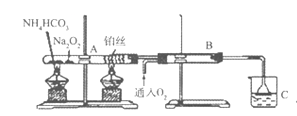
(1)被加热的铂丝处发生反应的化学方程式为_______________________________.
(2)B中出现的现象为___________________________.
(3)烧杯C中发生反应可得到酸X,如图:足量X的浓溶液与Cu反应,写出烧瓶中发生反应的离子方程式______________________.
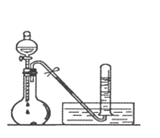
(4)实验完毕后,试管中收集到的气体的主要成分为______(写化学式).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性小组为了探究石蜡油(液态烷烃混合物)的分解产物,设计了如下实验方案。下列说法错误的是
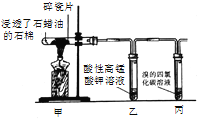
A. 石蜡油分解产物中含有烯烃,不含烷烃
B. 试管乙、丙中溶液均褪色,分别发生氧化反应、加成反应
C. 碎瓷片有催化和积蓄热量的作用
D. 结束反应时,为防止倒吸,先撤出导管,再停止加热
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com