
【题目】白铁皮在发生析氢腐蚀时有0.2mol电子转移,下列说法正确的是( )
A.有5.6 g金属被腐蚀
B.有6.5 g金属被氧化
C.有0.15 mol金属失去电子
D.标准状况下有4.48 L H2逸出
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某实验小组对含有Al3+的未知溶液进行了如下分析:
(1)滴加少量NaOH溶液,无明显变化;
(2)继续滴加NaOH溶液,有白色胶状沉淀生成;
(3)滴加过量的NaOH溶液,白色胶状沉淀明显减少。
实验小组经定量分析,得出如图所示沉淀的物质的量与滴加NaOH溶液体积的关系。下列说法错误的是 ( )
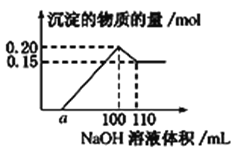
A. 该未知溶液中至少含有3种阳离子
B. NaOH溶液的物质的量浓度为5 mol·L-1
C. 若另一种离子为二价阳离子,则a=40
D. 若将最终沉淀过滤、洗涤、灼烧,其质量可能为6 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】判断下列盐溶液的酸碱性,能发生水解的用离子方程式表示,不能发生水解的请写上“不发生水解”字样.K2CO3溶液呈性;
K2SO4溶液呈性;
FeCl3溶液呈性 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国宋代《梦溪笔谈》中记叙了胆矾和铜的炼制过程:“信州铅山县有苦泉,煮之则得胆矾。熬胆矾铁釜,久之亦化为铜。”该炼制过程中没有涉及到的变化是( )
A. 复分解反应B. 氧化还原反应C. 置换反应D. 蒸发结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物E是制备镇静药安宁G的中间体,E和G的两种合成路线如下.(部分反应条件已略去)
已知: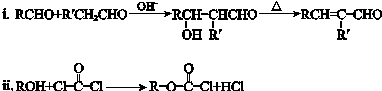
回答下列问题:
(1)A中所含官能团的名称是 , 检验该分子中官能团的常用试剂是 .
(2)A与C含有相同的官能团,B生成C的反应类型是 .
(3)C生成D的化学方程式是 .
(4)试剂a是 .
(5)下列说法正确的是 . a.E能发生取代反应、氧化反应和消去反应 b.M与K是同系物 c.1mol K能跟2molNaOH发生反应
(6)G的结构简式是 .
(7)在一定条件下E还能跟COCl2发生聚合反应生成高分子化合物,该反应的化学方程式是 .
(8)G的同分异构体P,分子中含有“ ![]() ”结构,P的核磁共振氢谱有5组峰,P能水解生成CH3CH2NH2和甲,1mol甲跟足量钠反应生成2mol H2 . 则P的结构简式是 .
”结构,P的核磁共振氢谱有5组峰,P能水解生成CH3CH2NH2和甲,1mol甲跟足量钠反应生成2mol H2 . 则P的结构简式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用纯溴和苯在铁离子催化下反应制取溴苯,得到粗溴苯后,要用如下操作精制,正确的操作顺序是( ) ①蒸馏 ②水洗分液 ③用干燥剂干燥 ④10%NaOH溶液洗分液
A.①②③④②
B.②④②③①
C.④②③①②
D.②④①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水系锂电池具有安全、环保和价格低廉等优点成为当前电池研究领域的热点.以钒酸钠(NaV3O8)为正极材料的电极反应式为:NaV3O8+xLi++xe﹣═NaLixV3O8 , 则下列说法不正确的是( ) 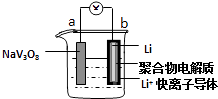
A.放电时,该电池的总反应为:xLi+NaV3O8═NaLixV3O8
B.充电过程中Li+从阳极向阴极迁移
C.充电过程中阳极的电极反应式为NaLixV3O8﹣xe﹣═NaV3O8+xLi+ , NaLixV3O8中钒的化合价发生变化
D.该电池可以用硫酸钠溶液作电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸是一种重要的化工原料,工业上生产硝酸的过程如下:
(1)以氮气、氢气为原料合成氨①下列措施可以提高H2的转化率是(填选项序号) .
a.选择适当的催化剂 b.增大压强 c.及时分离生成的NH3d.升高温度
②一定温度下,在密闭容器中充入1molN2和3molH2发生反应.若容器容积恒定,达到平衡状态时,容器内的压强是原来的 ![]() ,则N2的转化率a1=;
,则N2的转化率a1=;
若容器压强恒定,达到平衡状态时,N2的转化率为a2 , 则a2a1(填“>”、“<”或“=”)
(2)以氨气、空气为主要原料制硝酸.在容积恒定的密闭容器中进行反应2NO(g)+O2(g)2NO2(g)△H>0
该反应的反应速率(v)随时间(t)变化的关系如下图所示.若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号) . 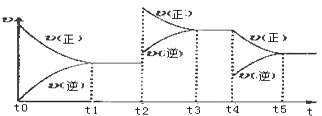
a.在t1~t2时,可依据容器内气体的压强保持不变判断反应已达到平衡状态
b.在t2时,采取的措施一定是升高温度
c.在t3~t4时,可依据容器内气体的密度保持不变判断反应已达到平衡状态
d.在t0~t5时,容器内NO2的体积分数在t3时值的最大
(3)硝酸厂常用如下2种方法处理尾气.①催化还原法:催化剂存在时用H2将NO2还原为N2 .
已知:2H2(g)+O2(g)=2H2O(g)△H=﹣483.6kJ/mol
N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol
则H2还原NO2生成水蒸气反应的热化学方程式是 .
②碱液吸收法:用Na2CO3溶液吸收NO2生成CO2 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有前四周期A、B、C、D、E、X六种元素,已知B、C、D、E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍.X原子的M能层上有4个未成对电子.请回答下列问题: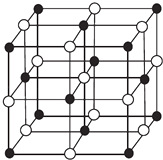
(1)写出C、D、E三种原子第一电离能由大到小的顺序为 . (用元素符号表示)
(2)A原子与B、C、D原子形成最简单化合物的稳定性由强到弱的顺序为(用分子式表示),根据价层电子对互斥理论预测BA2D的分子构型为 .
(3)某蓝色晶体,其结构特点是X2+、X3+离子分别占据六面体互不相邻的顶点,而六面体的每条棱上均有一个BC﹣ . 与A同族且相隔两个周期的元素R的离子位于立方体的恰当位置上.根据其结构特点可知该晶体的化学式为(用最简正整数表示) .
(4)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:
离子晶体 | NaCl | KCl | CaO |
晶格能/kJmol﹣1 | 786 | 715 | 3401 |
根据表格中的数据:判断KCl、MgO、TiN三种离子晶体熔点从高到低的顺序是 . MgO晶体中一个Mg2+周围和它最邻近且等距离的O2﹣有个.
(5)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和Cr2O3中,适合作录音带磁粉原料的是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com