
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
B.由C(石墨) C(金刚石) ΔH=+19 kJ·mol-1可知,金刚石比石墨稳定 C(金刚石) ΔH=+19 kJ·mol-1可知,金刚石比石墨稳定 |
C.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式为:H2(g)+ (g)====H2O(l) ΔH=+285.8 kJ·mol-1 (g)====H2O(l) ΔH=+285.8 kJ·mol-1 |
| D.在稀溶液中:H+(aq)+OH-(aq)====H2O(l) ΔH=-57.3 kJ·mol-1,若将0.5 mol浓硫酸溶液与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.水在高温加热后变成水蒸气 |
| B.生石灰变熟石灰 |
| C.石墨转变为金刚石 |
| D.钠投入水中 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.两种元素构成的共价化合物分子中的化学键都是极性键 |
| B.两种同种非金属元素原子间形成的化学键都是极性键 |
| C.含有极性键的化合物分子一定不含非极性键 |
| D.只要是离子化合物,其熔点就比共价化合物的熔点高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Zn(OH)2+2Ag____________________________________________。
Zn(OH)2+2Ag____________________________________________。 4CO2+2H2O__________________________________________________。
4CO2+2H2O__________________________________________________。 C6H12O6+6O2______________________________________________。
C6H12O6+6O2______________________________________________。 CaO+CO2↑______________________________________________________。
CaO+CO2↑______________________________________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 )
) 、CuSO
、CuSO 、Na
、Na CO
CO 中的一种或几种,现做以下实验:
中的一种或几种,现做以下实验: 溶液,产生白色沉淀。
溶液,产生白色沉淀。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 ⑧
⑧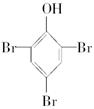


| A.①④⑥⑦⑨ | B.全溶 |
| C.除⑤⑧外全溶 | D.①④⑥⑦ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:判断题
 CO(g)+2H2(g) ΔH1=-36 kJ·mol-1
CO(g)+2H2(g) ΔH1=-36 kJ·mol-1 CO(g)+3H2(g) ΔH2="+216" kJ·mol-1
CO(g)+3H2(g) ΔH2="+216" kJ·mol-1查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 中一定正确的是( )
中一定正确的是( )| A.在离子化合物中不可能存在非极性共价键 |
| B.在共价化合物中不可能存在离子键 |
| C.离子化合物中一定含有金属元素和非金属元素 |
| D.非极性共价键只存在于双原子单质分子里 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com