
【题目】关于维生素的叙述中,不正确的是
A. 维生素是参与生物发育和新陈代谢所必需的一类小分子
B. 人体对维生素的需要量极小,但对人体的生长和健康至关重要
C. 为保证青少年的健康成长,应大量补充维生素
D. 习惯上把维生素分为脂溶性维生素和水溶性维生素
科目:高中化学 来源: 题型:
【题目】海水中有非常丰富的化学资源。
(一)从海水中提取镁可按如下步骤进行:①把贝壳制成石灰乳;②向引入的海水中加入石灰乳,沉降、洗涤、过滤沉淀物:③将沉淀物与盐酸反应,结晶、过滤、干燥;④加热,将MgCl2·6H2O晶体转化为无水MgCl2⑤电解得到产物。
(1)以上提取镁的全过程中,没有涉及的化学反应类型是__________(填字母)
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
(2)步骤中多次进行过滤,实验室进行过滤时用到的玻璃仪器主要有____________。
(3)某兴趣小组模拟步骤④设计下图装置进行实验,
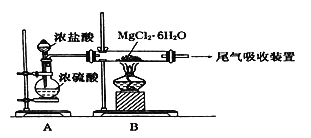
该装置中A的作用是______________________________________。
(4)下列关于提取镁的说法中,正确的是__________(填字母)
A.此法的优点之一是原料取自大海 B.进行①②③步骤的目的是富集MgCl2
C.可用电解熔融氧化镁的方法制取镁 D.将氯气循环利用,可提高经济效益
(二)从海水中得到的某氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按下图所示步骤进行操作。
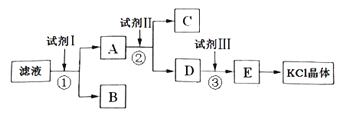
(1)起始滤液的pH________7 (填“大于”、“小于”或“等于”),其原因是(用离子方程式表示)__________________________________。
(2)试剂Ⅱ的化学式为___________,②中加入试剂Ⅱ的目的是_______________;③中发生反应的离子方程式为____________________;
(3)某冋学称取提纯的产品0.6984g,溶解后定容在100mL容量瓶中,每次取25,00mL
溶液,用0.1000mol·L-1的硝酸银标准溶液滴定,三次滴定消耗标准溶液的平均体积为22.50mL,该产品的纯度为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组热化学方程式中化学反应的ΔH前者大于后者的是( )
①C(s)+O2(g)=CO2(g) ΔH1 C(s)+![]() O2(g)===CO(g) ΔH2
O2(g)===CO(g) ΔH2
②S(s)+O2(g)=SO2(g) ΔH3 S(g)+O2(g)===SO2(g) ΔH4
③H2(g)+![]() O2(g)=H2O(l) ΔH5 2H2(g)+O2(g)===2H2O(l) ΔH6
O2(g)=H2O(l) ΔH5 2H2(g)+O2(g)===2H2O(l) ΔH6
④CaCO3(s)=CaO(s)+CO2(g) ΔH7 CaO+H2O(l)===Ca(OH)2(s) ΔH8
A. ①③④ B. ②③④ C. ①④ D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在酸性条件下有以下反应关系:
(i)KBrO3能将KI氧化成I2或KIO3 , 其本身被还原为Br2 .
(ii)Br2能将I-氧化为I2 .
(iii)KIO3能将I-氧化为I2 , 也能将Br-氧化为Br2 , 其本身被还原为I2 .
①上述物质中氧化剂氧化能力由强到弱的顺序是 .
②现向含有1molKI的硫酸溶液中加入含amolKBrO3的溶液,a的取值范围不同,所得产物也不同.试将讨论的结果填入下表.
编号 | a的取值范围 | 产物的化学式或(离子符号) |
A | I2 , Br- | |
B |
| |
C | a= | |
D | I2 , IO3- , Br2 | |
E | a≥ |
③若产物中碘单质和碘酸钾的物质的量相等,a的值为 .
④若a的值为1时,其产物及其物质的量分别为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把煤作为燃料可通过下列两种途径:
途径Ⅰ C(s) + O2(g) = CO2(g);ΔH = -393.15 kJ·mol-1 ①
途径Ⅱ 先制成水煤气:
C(s) + H2O(g) = CO(g) + H2(g); ΔH2 ②
再燃料水煤气:
2CO(g) + O2(g) = 2CO2(g); ΔH= -566kJ·mol-1 ③
2H2(g) + O2(g) = 2H2O(g);ΔH= -484 kJ·mol-1 ④
请回答下列问题:
(1)途径Ⅰ放出的热量理论上_________(填“大于”“等于”或“小于”)途径Ⅱ放出的热量。
(2)ΔH2=_______________。
(3)煤燃烧的烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为
NO(g)+O3(g)==NO2(g)+O2(g) ΔH=-200.9kJ·mol-1
NO(g)+![]() O2(g)==NO2(g) ΔH=-58.2kJ·mol-1
O2(g)==NO2(g) ΔH=-58.2kJ·mol-1
SO2(g)+O3(g)==SO3(g)+O2(g) ΔH=-241.6kJ·mol-1
反应3NO(g)+O3(g)==3NO2(g)的ΔH=________kJ·mol-1。
(4)已知下列各组热化学方程式
① Fe2O3(s)+3CO(g)=2Fe(s)+3CO2 △H=-25kJ/mol
② 3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47kJ/mol
③ Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640kJ/mol
请写出FeO(s)被CO(g)还原成Fe和CO2(g)的热化学方程式______________________________。
(5)在标准状况下的11.2L甲烷完全燃烧生成CO2 和液态水放出444.8kJ热量(298K),其燃烧热的热化学方程式______________________________________________________; 已知断裂下列1mol化学键需要吸收的能量分别为:C=O:745kJ/mol , O=O:496kJ/mol , C-H:414kJ/mol 则断裂1molH-O键需要提供的能量为____________________ kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,许多城市将公共汽车的燃料换成甲醇(CH3OH),以减少汽车尾气对环境造成的污染.
(1)某校研究性学习小组的同学为了探究甲醇在氧气中燃烧的产物,他们将甲醇在氧气中点燃,再用燃烧后的混合气体通过如下的装置进行实验(铁架台等装置已略去): 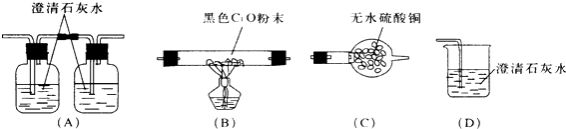
请你设计这些装置的连接顺序(装置不重复使用),使实验尽可能多地检验出甲醇燃烧的产物(用装置的编号表示);混合气体→、、→D.
(2)学习小组的同学通过正确的设计并进行实验,在实验过程中观察到的部分现象如下:
D和A中左边装置内的澄清石灰水均变浑浊,而A中右边装置内的澄清石灰水不变浑浊.请结合反应原理和实验现象进行分析,这次实验中甲醇的燃烧产物为 .
(3)通过该实验,请你谈谈应该怎样合理使用燃料 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于金属钠的性质描述不正确的是( )
A. 很软可用刀切割 B. 在空气中燃烧生成白色的过氧化钠
C. 金属钠通常保存在煤油里 D. 钠具有银白色金属光泽,密度比水小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某人体质较弱,经常因血糖低而头晕,为了防止发生危险,你应建议她随身携带富含哪种营养素的食品
A. 糖类 B. 蛋白质 C. 油脂 D. 矿物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示有关物质之间的转化关系,A,C,E,G为非金属单质,其中A,G常温常压下为气态,E遇淀粉变蓝,K是一种常用食品添加剂,L是常见的无色无味液体,I为淡黄色固体,J的焰色反应呈浅紫色(透过蓝色钴玻璃). 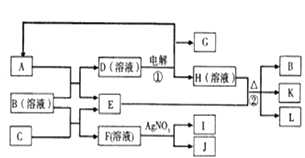
(1)B,I代表的物质化学式分别为、 .
(2)写出反应①②的离子方程式:
①
②
(3)选出实验室保存C单质的注意事项(A.无色瓶B.棕色瓶C.橡胶塞D.玻璃塞),除此之外还采取了什么特殊保存方法: .
(4)已知A,C,E均能与G反应,按其反应条件要求由高到低顺序为(用化学式表示)
(5)A与H溶液反应,其氧化产物和还原产物的物质的量的比为1:1,写出此反应的化学反应方程式: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com