
| A. | ①③④⑤⑦ | B. | ①②③④⑤⑦ | C. | ①②③④⑥ | D. | ①④⑥⑦ |
分析 HNO3在水中电离出的阳离子只有氢离子属于酸,完全电离的酸为强酸;
氧化物是两种元素组成其中一种为氧元素的化合物;
硝酸中含有氧元素,所以属于含氧酸;
酸电离的氢离子数判断几元酸;
电解质的概念分析,水溶液中或熔融状态下导电的化合物为电解质;
混合物是不同物质组成的;
根据组成元素分析,一般含碳元素的化合物为有机化合物;
解答 解:①HNO3水溶液中完全电离属于强酸,
②HNO3属是酸,不是氧化物,
③硝酸中含有氧元素,属于含氧酸,
④硝酸溶液中电离出一个氢离子,属于一元酸,
⑤硝酸水溶液中导电属于电解质,
⑥硝酸是一种物质组成,不是混合物,
⑦硝酸组成和性质分析,属于无机化合物,
故选A.
点评 本题主要考查物质的分类方法,解答时要分析物质的元素组成和物质组成,然后再根据各类物质概念的含义进行分析、判断,从而得出正确的结论,题目难度不大.


科目:高中化学 来源: 题型:实验题
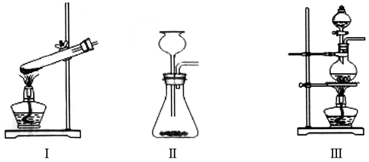
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
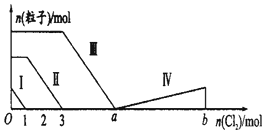 向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素.下列说法不正确的是( )
向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素.下列说法不正确的是( )| A. | 线段Ⅲ表示Br-的变化情况 | B. | 原溶液中n(FeI2):n(FeBr2)=1:3 | ||
| C. | 线段Ⅳ表示IO4-的变化情况 | D. | 根据图象可以计算a的值为6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用酒精萃取碘水中的碘 | |
| B. | 用蒸馏法进行海水淡化 | |
| C. | 用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 | |
| D. | 用加热-蒸发的方法可以除去粗盐中的CaCl2、MgCl2等杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 直径介于1nm~100nm之间的微粒称为胶体 | |
| B. | 电泳现象可以证明胶体粒子带电 | |
| C. | 丁达尔效应是溶液与胶体的本质区别 | |
| D. | 胶体粒子很小,可以透过滤纸和半透膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | D2O呈中性,PD=7 | |
| B. | 1LD2O溶液中含0.01molNaOD,PD=12 | |
| C. | 用D2O溶解0.1molDCl成1L溶液,PD=2 | |
| D. | 在100ml0.25mol/LDCl溶液中加入50ml0.2mol/L的NaOD的D2O溶液,PD=1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用蒸馏的方法将自来水制成蒸馏水 | B. | 用过滤的方法除去食盐水中的泥沙 | ||
| C. | 用淘洗的方法从沙里淘金 | D. | 用酒精萃取碘水中的碘 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+与Cl-数目比为2:3 | B. | Al3+与SO42-数目比为 3:2 | ||
| C. | Na+与Cl-数目比为1:1 | D. | Cl-与SO42-数目比为1:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com