


 ,除生成
,除生成 外,另一种产物是
外,另一种产物是 ,则A应为
,则A应为 ,B发生取代反应生成C,C发生取代反应然后酸化得到D,根据D分子式结合信息ii知,C结构简式为
,B发生取代反应生成C,C发生取代反应然后酸化得到D,根据D分子式结合信息ii知,C结构简式为 ,D结构简式为
,D结构简式为 ,邻醛基乙酸苯酯发生消去反应生成
,邻醛基乙酸苯酯发生消去反应生成 ,据此分析解答.
,据此分析解答. ,
, ;
; ,则A应为
,则A应为 ,B发生取代反应生成C,C发生取代反应然后酸化得到D,根据D分子式结合信息ii知,C结构简式为
,B发生取代反应生成C,C发生取代反应然后酸化得到D,根据D分子式结合信息ii知,C结构简式为 ,D结构简式为
,D结构简式为 ,邻醛基乙酸苯酯发生消去反应生成
,邻醛基乙酸苯酯发生消去反应生成 ,
, ,A→B的反应类型是取代反应,故答案为:
,A→B的反应类型是取代反应,故答案为: ;取代反应;
;取代反应; 与乙酸酐(
与乙酸酐( )反应,除生成
)反应,除生成 外,根据元素守恒可知,另一种产物是CH3COOH,
外,根据元素守恒可知,另一种产物是CH3COOH,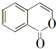 ,
, .
.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
A、Na2O2的电子式: |
B、K+的结构示意图: |
C、甲烷的比例模型: |
| D、丙烷分子的结构简式:CH3-CH2-CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol甲与足量的乙完全反应共转移2mol电子 |
| B、Y元素在周期表中的位置为第3周期ⅣA族 |
| C、原子半径:W>Y>Z>X |
| D、1.0L0.1mol?L-1戊溶液中阴离子总的物质的量小于0.1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙醇与乙酸都存在碳氧双键 |
| B、油脂水解可得到氨基酸和甘油 |
| C、淀粉和纤维素水解最终产物都是葡萄糖 |
| D、卤代烃加入硝酸酸化的硝酸银溶液可根据生成的卤化银沉淀颜色检验卤原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氟酸的电离方程式及热效应可表示为:HF(aq)?F-(aq)+H-(aq)△H=-10.4kJ?mol-1 |
| B、当V=20时,溶液中:c(OH-)=c(HF)+c(H+) |
| C、当V=20时,溶液中:c(F-)<c(Na+)=0.1mol?L-1 |
| D、当V>0时,溶液中可能存在:c(Na+)>c(F-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在一定条件下,对于反应mA(g)+n(B)?cC(g)+dD(g),C的百分含量(C%)与温度、压强的关系如图所示,下列该反应的△H、△S判断正确的是( )
在一定条件下,对于反应mA(g)+n(B)?cC(g)+dD(g),C的百分含量(C%)与温度、压强的关系如图所示,下列该反应的△H、△S判断正确的是( )| A、△H<0,△S>0 |
| B、△H>0,△S<0 |
| C、△H>0,△S>0 |
| D、△<0,△S<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、放出热量关系:a<b<196 |
| B、三个容器内反应的平衡常数:③>①>② |
| C、达平衡时SO3的体积分数:③>① |
| D、SO2的转化率:②>①>③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com