
【题目】一种碳纳米管能够吸附氢气,用这种材料制备的二次电池原理如下图所示,该电池的电解质为6 mol·L-1KOH溶液,下列说法中正确

A. 放电时K+移向负极
B. 放电时电池负极的电极反应为H2-2e-===2H+
C. 放电时电池正极的电极反应为NiO(OH)+H2O+e-===Ni(OH)2+OH-
D. 该电池充电时将碳电极与电源的正极相连
【答案】C
【解析】本题考查原电池和电解池工作原理。放电是原电池,阳离子向正极移动,阴离子向负极移动;充电是电解池,充电时阳极与电源正极相连,阴极与电源负极相连。
A.放电时,该电池为原电池,电解质溶液中阳离子向正极移动,所以K+移向镍电极,故A错误;B.已知电解质溶液为KOH溶液,放电时碳电极作负极,H2失电子发生氧化反应的电极式为:H2-2e-+OH-=2H2O,故B项错误;C.由图分析可知,放电时,镍电极为正极,NiO(OH)得电子发生还原反应,电极反应式为NiO(OH)+H2O+e-=Ni(OH)2+OH-,故C项正确;D.该电池充电时,碳电极得电子发生还原反应,作阴极,应与外接电源的负极相连,故D项错误。本题正确答案为C。


科目:高中化学 来源: 题型:
【题目】若NA表示阿伏加德罗常数,则下列说法不正确的是
A. 23g 钠在空气中充分燃烧,转移的电子数为NA
B. 50ml 12mol/L的盐酸与足量的MnO2共热,充分反应后,转移电子数为0.3NA
C. 0.6mol过氧化钠晶体中所含阴离子的数目为0.6NA
D. 常温常压下,8.8gN2O 和CO2混合气体所含的原子总数为0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知[Co(NH3)6]3+呈正八面体结构:各NH3分子间距相等,Co3+位于正八面的中心。若其中二个NH3分子被Cl-取代,所形成的[Co(NH3)4Cl2]+的同分异构体的种数有( )
A. 2种 B. 3种 C. 4种 D. 5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同温度和压强下,三个容积相同的容器中分别盛有N2、O2、空气,下列说法正确的是( )
A.三种气体质量之比为1∶1∶2B.三种气体的密度之比为1∶1∶1
C.三种气体的分子数之比为1∶1∶1D.三种气体原子数之比为1∶1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】共价键、金属键、离子键和分子间作用力都是构成物质微粒间的不同相互作用力,下列含有上述两种相互作用力的晶体是( )
A. 碳化硅晶体 B. Ar晶体
C. NaCl晶体 D. NaOH晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A.溶液能透过半透膜,而胶体和浊液均不能
B.胶体和其它分散系的本质区别是分散质粒子的大小
C.硫酸钡几乎不溶于水,所以它是非电解质
D.CO2溶于水能导电,但是它却是非电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将V1 mL 1.0mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,结果如图所示(实验中始终保持V1+V2=50mL).下列叙述正确的是( )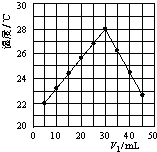
A.做该实验时环境温度为22℃
B.该实验表明化学能可以转化为热能
C.NaOH溶液的浓度约是1.00 mol/L
D.该实验表明有水生成的反应都是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验测得AlCl3为共价化合物,两个Al—Cl键间的夹角为120°。由此可见,AlCl3属于 ( )
A. 由极性键形成的极性分子
B. 由极性键形成的非极性分子
C. 由非极性键形成的极性分子
D. 由非极性键形成的非极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列有关说法正确的是
A. 2.0gH182O与D2O的混合物中所含中子数为NA
B. 标准状况下,22.4L二氯甲烷的分子数约为NA个
C. 1molH2与足量O2反应生成的H2O中含有的共价健总数为NA
D. 在11P4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4反应中,6molCuSO4能氧化白磷的分子数为1.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com