
科目:高中化学 来源: 题型:
| 加热前质量 | 加热前质量 | 加热后质量 |
| W1(容器) | W2(容器+晶体) | W3(容器+无水硫酸铜) |
| 160(W2-W3) |
| 18(W3-W1) |
| 160(W2-W3) |
| 18(W3-W1) |
| 0.418×2.35 |
| 0.025 |
| 0.418×2.35 |
| 0.025 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A.用98%的浓硫酸配制100 g 10%的稀硫酸溶液时,除使用量筒外还需用到容量瓶
B.用渗析法分离淀粉中混有的NaNO3杂质
C.无法用分液漏斗将乙二醇和水的混合液体分离
D.某无色溶液中加入盐酸产生无色无味气体,则溶液中一定含![]()
E.SO2、乙烯、乙炔通入溴水都能被氧化而使溴水褪色
F.用碱式滴定管量取20.00 mL 0.100 0 mol·L-1的KMnO4溶液
H.在中学“硫酸铜晶体里结晶水含量测定”的实验中,称量操作至少需要四次
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
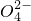 、Cl-等杂质______;
、Cl-等杂质______;| 加热前质量 | 加热前质量 | 加热后质量 |
| W1(容器) | W2(容器+晶体) | W3(容器+无水硫酸铜) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com