
物质 | 熔点/℃ | 沸点/℃ | 密度/(g/cm2) |
乙醇 | -144 | 78.0 | 0.789 |
乙酸 | 16.6 | 117.9 | 1.05 |
乙酸乙酯 | -83.6 | 77.5 | 0.009 |
浓H2SO4(98%) | — | 338 | 1.84 |

实验室制乙酸乙酯的主要步骤如下:①在20×
(1)步骤①中配制混合液时,向试管中加入三种试剂的顺序_______;
(2)如果使用的乙醇用18O标记,写出化学反应方程式____________________________;
(3)步骤②中必须用小火加热是依据表中的__________组数据;
A.熔点 B.沸点 C.密度
(4)步骤③在振荡前后观察到的现象是__________;
A.上层液体厚度变薄 B.下层液体红色变浅或无色
C.有气体产生 D.有果香味
解析:利用题给数据的暗示,结合浓H2SO4稀释的特性可知配制混合液时,应先向试管中加入乙醇(密度较小,与H2SO4混合时放热),再加入浓H2SO4,待适当冷却后再加入乙酸(浓H2SO4与乙醇混合所放出的热量可能引发乙酸与乙醇反应);因为乙酸乙酯的沸点与乙醇相近,所以反应时应用小火加热使其缓慢升温;乙醇、乙酸具有一定的挥发性,生成的乙酸乙酯中可能有少量的乙醇和乙酸,饱和Na2CO3溶液能吸收乙醇和乙酸,其中乙酸与Na2CO3能反应生成CO2气体,使Na2CO3溶液的碱性减弱。因为乙酸乙酯本身具有果香味,能明显闻到(不是看到)。振荡后乙酸乙酯中的乙醇、乙酸将明显减少,甚至被完全除去,但因其量较少,所以振荡后厚度变薄不易看出。
答案:(1)乙醇![]() 浓H2SO4
浓H2SO4![]() 乙酸
乙酸
(3)B
(4)BC


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:阅读理解
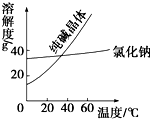 (1)阅读、分析下列两个材料:材料一:
(1)阅读、分析下列两个材料:材料一:| 物质 | 熔点/℃ | 沸点/℃ | 密度/g?cm3 | 溶解性 |
| 乙二醇(C2H6O2) | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意以互溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
阅读、分析下列材料:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
现有四组分散系:①汽油和水形成的乳浊液 ②含有泥沙的食盐水 ③溶有碘(I2)的碘化钾溶液 ④乙二醇和丙三醇混合溶液(乙二醇和丙三醇的部分物理性质见下表).
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 熔点/℃ | 沸点/℃ | 化学性质 | ||||
| S | 112.8 | 444.6 | 略 | ||||
| S2Cl2 | -77 | 137 | 遇水生成HCl、SO2、S;300℃以上发生反应:S2Cl2+Cl2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g?cm-3 | 溶解性 |
| 乙二醇 | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇 | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
A、 |
B、 |
C、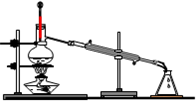 |
D、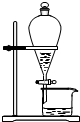 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com