
 2SO3��g������H��0
2SO3��g������H��0


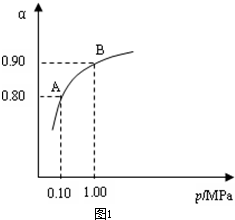
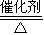 2SO3��g������H��0���÷�Ӧ������������ٵķ��ȷ�Ӧ�����ݻ�ѧƽ���ƶ�ԭ����֪�¶�Խ�ͣ�ѹǿԽ��ƽ��Խ��������У����������ת����Խ��ͨ��ͼ������ڳ�ѹ�£����������ת�����Ѿ��ܴ�����ѹǿ����߶��������ת������߲�������ѹǿ����豸�и��ߵ�Ҫ�����ӳɱ�������ͨ������¹�ҵ�����в��ó�ѹ����2.0mol SO2��1.0mol O2����5L�ܱ������У���Ӧ��ƽ�����ϵ��ѹǿΪ0.10M Pa����ͼ���Ͽ���֪�����������ת����Ϊ80%�����û�ѧƽ�������ʽ��ʽ���㣬��
2SO3��g������H��0���÷�Ӧ������������ٵķ��ȷ�Ӧ�����ݻ�ѧƽ���ƶ�ԭ����֪�¶�Խ�ͣ�ѹǿԽ��ƽ��Խ��������У����������ת����Խ��ͨ��ͼ������ڳ�ѹ�£����������ת�����Ѿ��ܴ�����ѹǿ����߶��������ת������߲�������ѹǿ����豸�и��ߵ�Ҫ�����ӳɱ�������ͨ������¹�ҵ�����в��ó�ѹ����2.0mol SO2��1.0mol O2����5L�ܱ������У���Ӧ��ƽ�����ϵ��ѹǿΪ0.10M Pa����ͼ���Ͽ���֪�����������ת����Ϊ80%�����û�ѧƽ�������ʽ��ʽ���㣬��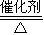 2SO3��g��
2SO3��g��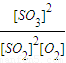 =
=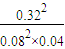 =400 L?mol-1
=400 L?mol-1

 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д� Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
| ���� |
| ���� |
| ���� |
| ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
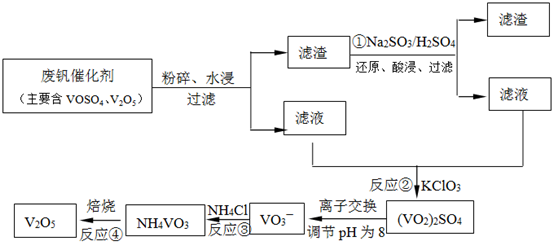
 ��ҵ���Ի�����Ϊԭ������������Ҫ��Ϊ�����ν��У������ա������������գ���ش����и����⣺
��ҵ���Ի�����Ϊԭ������������Ҫ��Ϊ�����ν��У������ա������������գ���ش����и����⣺| ���� | �� |
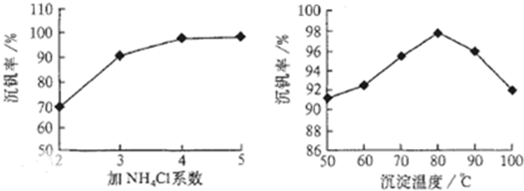
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
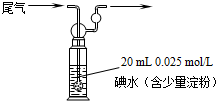
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com