
����Ŀ��ij���⻯ѧ��ȤС����������������ȡ������Al2O3���������ϵ�֪�����������Ҫ�ɷ���Al2O3��������Fe2O3��SiO2�ȡ�������������ȡAl2O3�Ĺ������£�
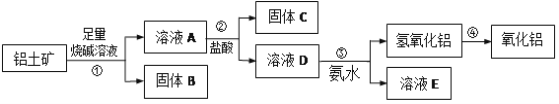
��1������B����Ҫ��;Ϊ��ֻдһ�ּ��ɣ�______��
��2���ڢٲ������������м��������ռ���Һ����ַ�Ӧ��������Ӧ�����ӷ���ʽ�ǣ�______
��3���ڢ۲���ʵ�����������______�������ϴ�ӵIJ�������______������A��Һ��ͨ������CO2�������ij���Ϊ______���ѧʽ����
��4����ҵ����ȡAlCl3����Al2O3��̿��Cl2�ڸ��������·�Ӧ����֪ÿ����0.5mol̿���ʣ�ת��1mol���ӣ���÷�Ӧ�Ļ�ѧ����ʽΪ______
���𰸡�����ԭ�ϡ�����Ϳ�ϡ������ Al2O3+2OH- =2AlO2- +H2O��SiO2+2OH- =SiO32-+ H2O ���� ������м�������ˮ����û���������ã���ˮ�������ظ�2~3�� Al (OH)3��H2SiO3 Al2O3+3Cl2+3C![]() 2 AlCl3+3CO
2 AlCl3+3CO
��������
���������м��������ռ���Һ�����������������������Һǿ��������ǿ�ֻFe2O3����ǿ�ᣬ�����ڼSiO2ֻ����ǿ��������ᣬ���ڢٵõ���Һ�к���ƫ��������ӡ���������ӣ���������������ɹ�����Ȼ������Ȼ�����Һ�е��백ˮ�������������������������ȷֽ⣬�������������ɴ˷������
(1)���������м��������ռ���Һ�����ڢٵõ���Һ�к���ƫ��������ӡ���������ӣ�����BΪ������������������Ϊ������ԭ�ϣ�������Ϊ��ɫ��������Ϳ�ϡ�����ȹʴ�Ϊ������ԭ�ϡ�����Ϳ�ϡ�����ȣ�
(2)���ݿ�ͼ���̣����������м��������ռ���Һ�����������������������Һǿ��������ǿ�Fe2O3ֻ����ǿ�ᣬ�����ڼSiO2ֻ����ǿ��������ᣬ���ڢٵõ���Һ�к���ƫ��������ӡ���������ӣ�����Ϊ���������������������м��������ռ���Һ������Ӧ�����ӷ���ʽ��Al2O3+2OH-=2AlO2-+H2O��SiO2+2OH-=SiO32-+H2O���ʴ�Ϊ��Al2O3+2OH-=2AlO2-+H2O��SiO2+2OH-=SiO32-+H2O��
(3)�Լ���Ϊ��ˮ���ܽ�������ת��Ϊ��������������������Ӧ�����ӷ���ʽΪ��Al3++3NH3��H2O=Al(OH)3��+3NH4+��ͨ�����˽�Al(OH)3�������������������м�������ˮ��ϴ�ӳ�����A��Һ���й�������Ӻ�ƫ��������ӣ�����A��Һ��ͨ������CO2���ᷢ����Ӧ�������ӷ���ʽΪ:AlO2-+CO2+2H2O=Al(OH)3��+HCO3-��SiO32-+2CO2+2H2O=H2SiO3��+2HCO3-�����ɵij���Ϊ����������������ʴ�Ϊ�����ˣ�������м�������ˮ����û���������ã���ˮ�������ظ�2~3�Σ�Al(OH)3��H2SiO3��
(4)Cl2��ǿ�����ԣ�̼���л�ԭ�ԣ�ÿ����0.5mol̼���ʣ�ת��1mol���ӣ���˵����Ӧ��̼ʧȥ2�����ӣ�������������CO�����Է�Ӧ�Ļ�ѧ����ʽ��Al2O3+3Cl2+3C![]() 2AlCl3+3CO���ʴ�Ϊ��Al2O3+3Cl2+3C
2AlCl3+3CO���ʴ�Ϊ��Al2O3+3Cl2+3C![]() 2AlCl3+3CO��
2AlCl3+3CO��


 ѧҵ����һ��һ��ϵ�д�
ѧҵ����һ��һ��ϵ�д� Сѧ��ʱ��ҵȫͨ����ϵ�д�
Сѧ��ʱ��ҵȫͨ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2L�����ܱ�������Ͷ������M��s����һ������R��g����������ӦΪM��s��+R��g��![]() X��g��+Y��g�� ��H������ʵ�����������ʾ��
X��g��+Y��g�� ��H������ʵ�����������ʾ��
ʵ�� | �¶�/�� | ��ʼʱR�����ʵ���/mol | ƽ��ʱ���������ʵ���/mol |
�� | 300 | 2.00 | 2.80 |
�� | 400 | 2.00 | 3.00 |
�� | 400 | 4.00 | a |
�����ƶ���ȷ���ǣ� ��
A.������Ӧ�У���H��0
B.ʵ����У��÷�Ӧ��ƽ�ⳣ��K=0.5
C.ʵ��پ�4min�ﵽƽ�⣬0��4 min������X��=0.2mol��L-1��min-1
D.ʵ�����a=6.00
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳ��ݣ�Gelsemium��Ϊ�й��Ŵ��Ŵ�ҩ֮һ���ݼ���������Ѫ��������ִ��������Ǻ����ٿ�ֲ������٣����еĶ��غܶ࣬�����Ƿ�����������ֶ��صĽṹ��ʽ�������ƶ���ȷ���ǣ�������
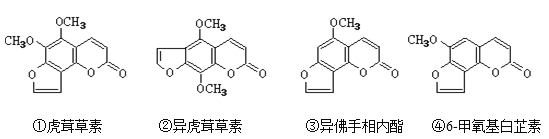
A.������������������Ȣ��ж�
B.�١��ܻ�Ϊͬϵ��
C.�١��ڡ��ۡ��ܾ���������������Һ��Ӧ
D.�����ʵ����ڡ��۷ֱ���������������ȫȼ�գ�ǰ�����������Ⱥ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��C��N��Si���γɶ��ָ�Ӳ�Ȳ��ϣ���![]() ��
��![]() ��SiC
��SiC

��1��![]() ��
��![]() ��Ӳ�Ƚϸߵ���______��������______��
��Ӳ�Ƚϸߵ���______��������______��
��2��![]() ��N���γ�һ����ʯī�ṹ���ϣ���ϳɹ�����ͼ1��ʾ������ʯī�ṹ���ϻ�����Ļ�ѧʽΪ______����ϳɹ������������谷�γɣ������谷��Nԭ�ӵ��ӻ���ʽ��______��
��N���γ�һ����ʯī�ṹ���ϣ���ϳɹ�����ͼ1��ʾ������ʯī�ṹ���ϻ�����Ļ�ѧʽΪ______����ϳɹ������������谷�γɣ������谷��Nԭ�ӵ��ӻ���ʽ��______��
��3��![]() ��N���γ�һ����Ԫ��״�л�������
��N���γ�һ����Ԫ��״�л�������![]() ��дΪ
��дΪ![]() ����ṹΪ
����ṹΪ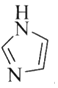
![]() ������
������![]() �Ľṹʾ��ͼ��ͼ2��
�Ľṹʾ��ͼ��ͼ2��
��������![]() ��
��![]() ֮������������Ӽ�ľ������������������������д��������ı�ʾʽ��______��
֮������������Ӽ�ľ������������������������д��������ı�ʾʽ��______��![]() ����ˮ������ı�ʾʽΪ
����ˮ������ı�ʾʽΪ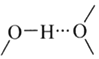
![]()
�ڶ�ԭ�ӷ����и�ԭ������ͬһƽ�棬�����ƽ�е�p�������p���ӿ��ڶ��ԭ�Ӽ��˶����γ�������![]() ��������
��������![]() �������������
�������������![]() ����
����![]() ����im�����д��ڵ�������
����im�����д��ڵ�������![]() ������______��
������______��
��4��![]() Ϊ������ϵ���壬�þ�����ԭ�ӵ��������Ϊ
Ϊ������ϵ���壬�þ�����ԭ�ӵ��������Ϊ
C��![]() ��
��![]() ��
��![]() 0��
0��![]() ��
��![]() ��
��![]() ��
��![]()
Si��![]() ��
��![]() ��
��![]() ��
��![]()
��![]() ���������к���______��Siԭ�ӡ�______��Cԭ�ӡ�
���������к���______��Siԭ�ӡ�______��Cԭ�ӡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������̼��Ԫ�صĵ��ʼ��仯�����ڻ���ҽҩ�����ϵ��������Ź㷺��Ӧ�ã��ش��������⣺
��1��![]() �������������������غ���
�������������������غ���![]() ��
��![]() ����һ����Ҫ�������û�������
����һ����Ҫ�������û�������![]() �ĺ�������Ų�ʽΪ____�������ǽ���Ԫ�صĵ縺���ɴ�С��˳��Ϊ___
�ĺ�������Ų�ʽΪ____�������ǽ���Ԫ�صĵ縺���ɴ�С��˳��Ϊ___![]() ̼ԭ��Ϊ____�ӻ���
̼ԭ��Ϊ____�ӻ���![]() �Ŀռ乹��Ϊ_____��
�Ŀռ乹��Ϊ_____��
��2�����ط�����![]() ��
��![]() ������Ŀ֮��_____��
������Ŀ֮��_____��
��3��Ŀǰ���ֵ���ԭ�Ӵ�![]() ��������±�����ƣ���ԭ�Ӵ�
��������±�����ƣ���ԭ�Ӵ�![]() ����____���壮
����____���壮![]() ���ڵĻ�ѧ����_____
���ڵĻ�ѧ����_____![]() ����ĸ
����ĸ![]() ��
��
A.���Ӽ� ![]() ���Լ�
���Լ� ![]() �Ǽ��Լ�
�Ǽ��Լ� ![]() ��λ��
��� ![]() ���
��� ![]() ������
������
��4����֪��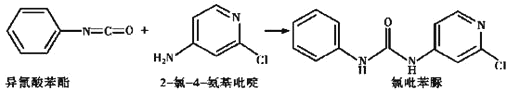 ����Ӧ��
����Ӧ��![]() ��_____��
��_____��![]() ��_____
��_____![]() ��������������������
��������������������![]() ��
��
��5����ԭ�ӷ����и�ԭ������ͬһƽ�棬�����ƽ�е�p�������p���ӿ��ڶ��ԭ�Ӽ��˶����γ�������![]() ��������
��������![]() �������������
�����д���������![]() �������ɱ�ʾ��
�������ɱ�ʾ��![]() ����
����![]()
![]() ����
����![]() �������
�е�������![]() �����ɱ�ʾΪ_________
�����ɱ�ʾΪ_________
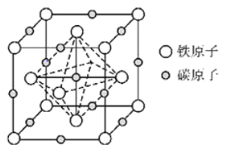
��6����������̼�ܽ���![]() ���γɵ�һ�ּ�϶�����壬����Ϊ���������ṹ����ͼ��ʾ���������ܶ�Ϊ
���γɵ�һ�ּ�϶�����壬����Ϊ���������ṹ����ͼ��ʾ���������ܶ�Ϊ![]() ���������������̼ԭ��֮��ľ���Ϊ______
���������������̼ԭ��֮��ľ���Ϊ______![]() �����ӵ�������ֵ��
�����ӵ�������ֵ��![]() ��ʾ��д����ļ���ʽ����
��ʾ��д����ļ���ʽ����![]() ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ϩ����������������Zn������ˮ�⣬�ɵõ�ȩ��һ���л���ͪ���磺
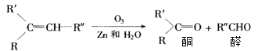
���л�ѧʽC7H14��ϩ������H2��ȫ�ӳɺ�IJ���˴Ź�������������壬�ҷ����֮��Ϊ9:6:1������������ϩ����O3��������Zn������ˮ��IJ��ﹲ�����м���(�����������칹)( )
A. 2��B. 4��C. 5��D. 6��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����Ʊ���������ʵ��װ����ͼ��ʾ(�г�װ������ȥ)������˵������ȷ����

A.ˮԡ���ȵ��ŵ���ʹ��Ӧ�����Ⱦ��ȡ��������¶�
B.��Ӧ��ȫ��,��������a��b����õ���Ʒ
C.ʵ�����������������b��δ�������Ƭ,����ȴ��
D.��Ũ���ᡢŨ����ͱ����ʱ,Ӧ��Ũ�����м���Ũ����, ����ȴ�����º�,�����û������뱽��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ú�п��������Ҫ��Zn�Լ�����S��Fe��Mn��Cd�ȣ���ȡ����п��ZnO���Ĺ���������ͼ
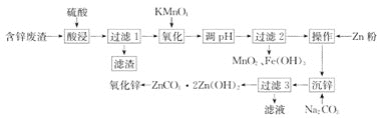
�ش��������⣺
��1���������ʱ��п�����Ľ�������ͼ��a����ʾ��Ӧ���ƽ�ȡ�յ��pHΪ________��
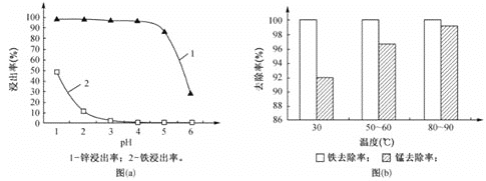
��2����������ʱ��Fe2+��Mn2+ȥ�������¶ȵĹ�ϵ��ͼ��b����ʾ����ͬ�����»�ԭ�Խ�ǿ����________������Fe2+������Mn2+������Fe2+��KMnO4��������Fe3+��MnO2�����ӷ���ʽΪ________��
��3����Zn������������Ŀ����________��
��4������п�������ӷ���ʽΪ________���ɼ�ʽ̼��п�Ʊ���������п�ķ�����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.1mol/L NaOH��Һ�ζ�20mL 0.1mol/L CH3COOH��Һ�ĵζ�������ͼ������˵��������ǣ�

A.�����ʾ��Һ�У�c(CH3COO��)��c(CH3COOH)��c(Na+)��c(H+)��c(OH��)
B.�����ʾ��Һ�У�c(Na+)=c(CH3COO��)��c(H+)=c(OH��)
C.��٢ڢ���ʾ��Һ�У���������c(Na+)+c(H+)=c(CH3COO��)+c(OH��)
D.��۱�ʾ�����ζ�����ǡ�ôﵽ�ζ��յ㣬�ڹ�������Һ��![]() ʼ�ղ���
ʼ�ղ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com