
分析 金属与硝酸反应生成硝酸盐和氮的氧化物,被还原的硝酸的物质的量等于生成气体的物质的量,根据反应中消耗硝酸的物质的量结合质量守恒列方程组可计算合金中银的质量分数,以此来解答.
解答 解:(1)被还原的硝酸的物质的量等于生成气体的物质的量,即:n(HNO3)(被还原)=$\frac{6.72L}{22.4L/mol}$=0.3mol,
答:被还原的硝酸的物质的量为0.3mol.
(2)剩余硝酸的物质的量为n(HNO3)(剩余)=0.08L×1mol/L=0.08mol,
参加反应的硝酸为:0.08L×13.5mol/L-0.08mol=1mol,
设混合物中含有xmolAg,ymolCu,
则有$\left\{\begin{array}{l}{106x+64y=30.0(质量守恒)}\\{x+2y+0.3+0.08=1.08(N元素守恒)}\end{array}\right.$
解之得:x=0.1,y=0.3
则:m(Ag)=0.1mol×108g/mol=10.8g,
合金中银的质量分数为$\frac{10.8g}{30.0g}$=36.0%.
答:合金中银的质量分数为36.0%.
点评 本题考查氧化还原反应的计算,为高频考点,把握原子守恒、质量守恒的为解答的关键,侧重分析与计算能力的考查,注意守恒法可避免书写化学方程式的繁琐,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
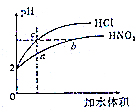 室温下,体积和pH都相同的盐酸和HNO2溶液加水稀释时的pH变化曲线如图所示,下列有关说法正确的是( )
室温下,体积和pH都相同的盐酸和HNO2溶液加水稀释时的pH变化曲线如图所示,下列有关说法正确的是( )| A. | 原HNO2溶液的浓度为0.01mol•L-1 | |
| B. | 溶液中水的电离程度:b>c | |
| C. | $\frac{c(N{{O}_{2}}^{-})}{c(HN{O}_{2})•c(O{H}^{-})}$比值:b>a | |
| D. | 等浓度的HNO2与NaOH溶液按体积比为2:1充分反应的混合液中,c(NO2-)+2c(OH-)=c(HNO2)+2c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 往紫色石蕊试液中加入盐酸,溶液变红 | |
| B. | 饱和FeCl3溶液在沸水中变成红褐色胶体 | |
| C. | 向FeSO4溶液中滴加NaOH溶液,生成的沉淀由白色变成灰绿色,最后变成红褐色 | |
| D. | SO2使滴有酚酞的NaOH溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 己烷(己烯) | 溴水 | 分液 |
| B | 淀粉溶液(NaCl) | 水 | 过滤 |
| C | CH3CH2OH(CH3COOH) | CaO | 蒸馏 |
| D | CO2(SO2) | Na2CO3溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
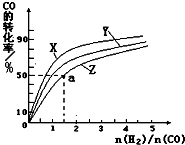 甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产.工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ•mol-1
甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产.工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ•mol-1| 0min | 5min | 10min | |
| CO | 0.1 | 0.05 | |
| H2 | 0.2 | 0.2 | |
| CH3OH | 0 | 0.04 | 0.05 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
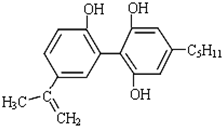
| A. | 一定条件下1mol该物质能与1molH2发生加成反应 | |
| B. | 该有机物能与FeCl3溶液发生显色反应 | |
| C. | 该有机物能与碳酸氢钠溶液反应 | |
| D. | 该有机物是苯酚的同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=14的溶液中:NH4+、Al3+、Cl-、NO3- | |
| B. | 中性溶液中:Fe2+、K+、Cl-、${SO}_{4}^{2-}$ | |
| C. | 含有大量Ba2+的溶液中:Mg2+、Na+、${NO}_{3}^{-}$、Cl- | |
| D. | 由水电离出的c(H+)=1×10-12mol-1的溶液中:Na+、Mg2+、HCO3-、CH3COO- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com