
下列各溶液中,Na+浓度最大的是( )
|
| A. | 5L 1.2mol•L﹣1的Na2SO4溶液 |
|
| B. | 2L 0.8mol•L﹣1的NaOH溶液 |
|
| C. | 1L 1mol•L﹣1的Na2CO3溶液 |
|
| D. | 4L 0.5mol•L﹣1的NaCl溶液 |
考点:
物质的量浓度.
专题:
物质的量浓度和溶解度专题.
分析:
电解质离子的浓度=电解质浓度×电解质电离出该离子的数目,与溶液的体积无关,据此结合选项判断.
解答:
解:A、5L 1.2mol•L﹣1的Na2SO4溶液中Na+浓度为1.2mol/L×2=2.4mol/L;
B、2L 0.8mol•L﹣1的NaOH溶液中Na+浓度为0.8mol/L×1=0.8mol/L;
C、1L 1mol•L﹣1的Na2CO3溶液中Na+浓度为1mol/L×2=2mol/L;
D、4L 0.5mol•L﹣1的NaCl溶液中Na+浓度为0.5mol/L×1=0.5mol/L;
所以Na+浓度最大的是A,
故选A.
点评:
本题考查离子的物质的量浓度,注意电解质溶液中离子的浓度与电解质浓度的计算.


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
影响化学反应速率与平衡的因素有多方面,如浓度压强温度催化剂等.下列有关说法不正确的是( )
|
| A. | 其它条件不变时,改变压强能改变气体反应的速率,但不一定改变平衡 |
|
| B. | 增大浓度能加快化学反应速率,原因是增大浓度就增加了反应体系中活化分子的百分数 |
|
| C. | 温度升高使化学反应速率加快的主要原因是增加了反应体系中活化分子的百分数 |
|
| D. | 加入催化剂能降低反应所需的活化能,使反应速率加快,平衡常数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各溶液中,Na+浓度最大的是( )
|
| A. | 5L 1.2mol•L﹣1的Na2SO4溶液 |
|
| B. | 2L 0.8mol•L﹣1的NaOH溶液 |
|
| C. | 1L 1mol•L﹣1的Na2CO3溶液 |
|
| D. | 4L 0.5mol•L﹣1的NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是( )

|
| A. | 蒸馏、蒸发、萃取、过滤 | B. | 蒸馏、过滤、萃取、蒸发 |
|
| C. | 萃取、过滤、蒸馏、蒸发 | D. | 过滤、蒸发、萃取、蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是( )
|
| A. | 0.012kg 12C含有的12C是NA个 |
|
| B. | NA个水分子的质量是18g/mol |
|
| C. | 1mol O2中含有的氧气分子数为NA个 |
|
| D. | 含有NA个氧原子的H2SO4的物质的量是0.25mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数,下列叙述正确的是( )
|
| A. | 标准状况下,22.4LH2O含有的分子数为NA |
|
| B. | 常温常压下,1.06gNa2CO3含有的Na+离子数为0.02 NA |
|
| C. | 通常状况下,1 NA个CO2分子占有的体积为22.4L |
|
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,Cl﹣离子个数为0.02 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)同温同压下,同体积的甲烷(CH4)和二氧化碳分子数之比为 ,物质的量之比为 ,原子总数之比为 ,密度之比为 .
(2)在标准状况下,4g H2、11.2L O2、1mol H2O中,所含分子数最多的是 ,含原子数最多的是 ,体积最小的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知:pM=﹣lgc(M),p(CO32﹣)=﹣lgc(CO32﹣).下列说法正确的是()
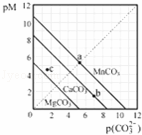
A. MgCO3、CaCO3、MnCO3的Ksp依次增大
B. a点可表示MnCO3的饱和溶液,且c(Mn2+)<c(CO32﹣)
C. b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32﹣)
D. c点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO32﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
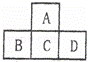
有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素的原子核外共有56个电子,在周期表中的位置如图所示.E元素的最高价氧化物既能与强酸反应又能与强碱反应.请回答:
(1)写出下列元素的元素符号:A 、B 、D .
(2)A元素与氢元素形成的H2A化合物分子中,所含化学键为 键(填“离子”或“极性”或“非极性”),用电子式表示H2A的形成过程 , .
(3)A元素与E元素形成的化合物的化学式是 ,该化合物在物质分类中属于 氧化物.(填“酸性”,“碱性”或“两性”)
(4)向D元素与E元素形成的化合物的水溶液中滴加NaOH溶液,开始时,实验现象是 有 ,反应的离子方程式为 ;继续滴加NaOH溶液至过量,实验现象是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com