
 Ņ¹Ä»½µĮŁ£¬±±¾©°ĀŌĖ»įÖ÷»į³””°Äń³²”±ÄŚµĘ»š»Ō»Ķ£¬¹ÄÉŖĘėĆł£®čč²µÄŃĢ»ØŌŚæÕÖŠ×é³É°ĀŌĖĪå»·µČĶ¼°ø£¬Óė³”ÄŚ±ķŃŻĻąŗōÓ¦£®Äń³²Ņ¹¾°ÕÕĆ÷ÓÉĪåøö²æ·Ö×é³É£¬ĘäÖŠÖ÷ĢåÕÕĆ÷ŅŌ“«Ķ³ĪÄ»ÆŌŖĖŲ”°ÖŠ¹śŗģ”±ĪŖÖ÷É«£®ČēĶ¼1ŹĒ±±¾©Äń³²ŹŌ·ÅŃĢ»š°ĀŌĖĪå»·Ķ¼£¬²¢»Ų“šĻĀĮŠĪŹĢā£ŗ
Ņ¹Ä»½µĮŁ£¬±±¾©°ĀŌĖ»įÖ÷»į³””°Äń³²”±ÄŚµĘ»š»Ō»Ķ£¬¹ÄÉŖĘėĆł£®čč²µÄŃĢ»ØŌŚæÕÖŠ×é³É°ĀŌĖĪå»·µČĶ¼°ø£¬Óė³”ÄŚ±ķŃŻĻąŗōÓ¦£®Äń³²Ņ¹¾°ÕÕĆ÷ÓÉĪåøö²æ·Ö×é³É£¬ĘäÖŠÖ÷ĢåÕÕĆ÷ŅŌ“«Ķ³ĪÄ»ÆŌŖĖŲ”°ÖŠ¹śŗģ”±ĪŖÖ÷É«£®ČēĶ¼1ŹĒ±±¾©Äń³²ŹŌ·ÅŃĢ»š°ĀŌĖĪå»·Ķ¼£¬²¢»Ų“šĻĀĮŠĪŹĢā£ŗ £¬C”¢D¾łĪŖŌ×Ó¾§Ģ壬CÓė“æ¼īŌŚøßĪĀĻĀµÄ·“Ó¦ŹĒ¹¤ŅµÖĘ²£Į§µÄÖ÷ŅŖ·“Ó¦Ö®Ņ»£¬DÖŠĖłŗ¬Į½ÖÖŌŖĖŲµÄŌ×ÓøöŹż±ČĪŖ3£ŗ4£¬µē×Ó×ÜŹżÖ®±ČĪŖ3£ŗ2£®øł¾ŻŅŌÉĻŠÅĻ¢»Ų“šĻĀĮŠĪŹĢā£ŗ
£¬C”¢D¾łĪŖŌ×Ó¾§Ģ壬CÓė“æ¼īŌŚøßĪĀĻĀµÄ·“Ó¦ŹĒ¹¤ŅµÖĘ²£Į§µÄÖ÷ŅŖ·“Ó¦Ö®Ņ»£¬DÖŠĖłŗ¬Į½ÖÖŌŖĖŲµÄŌ×ÓøöŹż±ČĪŖ3£ŗ4£¬µē×Ó×ÜŹżÖ®±ČĪŖ3£ŗ2£®øł¾ŻŅŌÉĻŠÅĻ¢»Ų“šĻĀĮŠĪŹĢā£ŗ·ÖĪö £Ø1£©ŃĢ»šĀķÉĻĮŖĻėµ½²æ·Ö½šŹōµÄŌŖĖŲµÄŃęÉ«·“Ó¦£¬ĖüŹĒĶā²ćµē×ӵļ¤·¢¶ų·¢³öµÄ£¬ŹĒĪļĄķ±ä»Æ£»
£Ø2£©ÓÉŠÅĻ¢ÖŖµĄÖ»ÓŠĀČŌŖĖŲµÄ»ÆŗĻ¼Ū·¢Éś±ä»Æ£¬KClO3·¢ÉśĘē»Æ·“Ó¦ĪŖKClO4ŗĶClO2£¬»¹ÓŠKHSO4Éś³É£»
£Ø3£©AŹĒÕÓĘųµÄÖ÷ŅŖ³É·Ö£¬ĪŖ¼×Ķ飻B·Ö×ÓÖŠĖłŗ¬µē×ÓŹżĪŖ18£¬B²»ĪČ¶Ø£¬¾ßÓŠ½ĻĒæµÄŃõ»ÆŠŌ£¬ĘäĻ”ČÜŅŗŹĒŅ½ĮĘÉĻ¹ć·ŗŹ¹ÓƵÄĻū¶¾¼Į£¬æÉÖŖBĪŖH2O2£»BÓėCĻą½»µÄ²æ·ÖĪŖOŌŖĖŲ£¬CÓė“æ¼īŌŚøßĪĀĻĀµÄ·“Ó¦ŹĒ¹¤ŅµÖĘ²£Į§µÄÖ÷ŅŖ·“Ó¦Ö®Ņ»£¬¹ŹCĪŖSiO2£»E·Ö×ÓÖŠĖłŗ¬µē×ÓŹżĪŖ18£¬EŹĒÓÉĮłøöŌ×Ó¹¹³ÉµÄ·Ö×Ó£¬Ō×ÓĘ½¾łµē×ÓŹżĪŖ3£¬¹ŹEÖŠŗ¬ÓŠHŌŖĖŲ£¬EĪŖN2H4£»DÖŠŗ¬ÓŠSiŌŖĖŲ£¬»¹ŗ¬ÓŠHŌŖĖŲ»ņNŌŖĖŲ£¬ÓÉDÖŠĖłŗ¬µÄĮ½ÖÖŌŖĖŲµÄŌ×ÓøöŹżÖ®±ČĪŖ3£ŗ4£¬¹ŹDĪŖSi3N4£®
½ā“š ½ā£ŗ£Ø1£©ŃĢ»šĀķÉĻĮŖĻėµ½²æ·Ö½šŹōµÄŌŖĖŲµÄŃęÉ«·“Ó¦£¬ĖüŹĒĶā²ćµē×ӵļ¤·¢¶ų·¢³öµÄ£¬ŹĒĪļĄķ±ä»Æ£¬
¹Ź“š°øĪŖ£ŗŃęÉ«£»ĪļĄķ£»
£Ø2£©ÓÉŠÅĻ¢ÖŖµĄÖ»ÓŠĀČŌŖĖŲµÄ»ÆŗĻ¼Ū·¢Éś±ä»Æ£¬KClO3·¢ÉśĘē»Æ·“Ó¦ĪŖKClO4ŗĶClO2£¬»¹ÓŠKHSO4Éś³É£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗ3KClO3+2H2SO4£ØÅØ£©=2KHSO4+KClO4+H2O+2ClO2”ü£¬
¹Ź“š°øĪŖ£ŗ3KClO3+2H2SO4£ØÅØ£©=2KHSO4+KClO4+H2O+2ClO2”ü£»
£Ø3£©AŹĒÕÓĘųµÄÖ÷ŅŖ³É·Ö£¬ĪŖ¼×Ķ飻B·Ö×ÓÖŠĖłŗ¬µē×ÓŹżĪŖ18£¬B²»ĪČ¶Ø£¬¾ßÓŠ½ĻĒæµÄŃõ»ÆŠŌ£¬ĘäĻ”ČÜŅŗŹĒŅ½ĮĘÉĻ¹ć·ŗŹ¹ÓƵÄĻū¶¾¼Į£¬æÉÖŖBĪŖH2O2£»BÓėCĻą½»µÄ²æ·ÖĪŖOŌŖĖŲ£¬CÓė“æ¼īŌŚøßĪĀĻĀµÄ·“Ó¦ŹĒ¹¤ŅµÖĘ²£Į§µÄÖ÷ŅŖ·“Ó¦Ö®Ņ»£¬¹ŹCĪŖSiO2£»E·Ö×ÓÖŠĖłŗ¬µē×ÓŹżĪŖ18£¬EŹĒÓÉĮłøöŌ×Ó¹¹³ÉµÄ·Ö×Ó£¬Ō×ÓĘ½¾łµē×ÓŹżĪŖ3£¬¹ŹEÖŠŗ¬ÓŠHŌŖĖŲ£¬EĪŖN2H4£»DÖŠŗ¬ÓŠSiŌŖĖŲ£¬»¹ŗ¬ÓŠHŌŖĖŲ»ņNŌŖĖŲ£¬ÓÉDÖŠĖłŗ¬µÄĮ½ÖÖŌŖĖŲµÄŌ×ÓøöŹżÖ®±ČĪŖ3£ŗ4£¬¹ŹDĪŖSi3N4£®
¢ŁBĪŖH2O2µÄĖ®ČÜŅŗ³ŹČõĖįŠŌ£¬ĘäÖ÷ŅŖµÄµēĄė·½³ĢŹ½æɱķŹ¾ĪŖ£ŗH2O2?HO2-+H+£¬DĪŖSi3N4£»
¹Ź“š°øĪŖ£ŗH2O2?HO2-+H+£»Si3N4£»
¢ŚA”¢B”¢EÖŠ¾łŗ¬ÓŠµÄŅ»ÖÖŌŖĖŲĪŖHŌŖĖŲ£¬¹Ź“š°øĪŖ£ŗH£»£®
¢ŪCÓė“æ¼ī·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗSiO2+Na2CO3$\frac{\underline{\;øßĪĀ\;}}{\;}$Na2SiO3+CO2”ü£¬
¹Ź“š°øĪŖ£ŗSiO2+Na2CO3$\frac{\underline{\;øßĪĀ\;}}{\;}$Na2SiO3+CO2”ü£»
¢ÜŅŗĢ¬BĪŖH2O2£¬ŅŗĢ¬EĪŖN2H4£¬¶žÕß·“Ó¦æÉÉś³ÉŅ»ÖÖĘųĢ¬µ„ÖŹŗĶŅ»ÖÖ³£¼ūŅŗĢå£¬Éś³ÉµÄĘųĢåĪŖµŖĘų”¢ŅŗĢåĪŖĖ®£¬1molB²Ī¼Ó·“Ó¦·Å³öČČĮæQkJ£¬·“Ó¦ČČ»Æѧ·½³ĢŹ½ĪŖ£ŗN2H4£Øl£©+2H2O2£Øl£©=N2£Øg£©+4H2O£Øl£©”÷H=-2Q kJ/mol£¬
¹Ź“š°øĪŖ£ŗN2H4£Øl£©+2H2O2£Øl£©=N2£Øg£©+4H2O£Øl£©”÷H=-2Q kJ/mol£®
µćĘĄ ±¾Ģāæ¼²éĪŽ»śĪļµÄĶʶĻ”¢ŃęÉ«·“Ó¦”¢»Æѧ·½³ĢŹ½ŹéŠ“µČ£¬ÄŃ¶Č½Ļ“ó£¬ÕĘĪÕ³£¼ū18µē×ÓĪļÖŹŹĒĶʶĻµÄ¹Ų¼ü£¬ŠčŅŖѧɜ¶Ō³£¼ūĪļÖŹµÄ½į¹¹ÓėŠŌÖŹŹģĮ·ÕĘĪÕ£®


 Č«Óųå“Ģ100·ÖĻµĮŠ“š°ø
Č«Óųå“Ģ100·ÖĻµĮŠ“š°ø Ó¢²Åµć½ņĻµĮŠ“š°ø
Ó¢²Åµć½ņĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
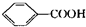 ·“Ó¦£®
·“Ó¦£® $”ś_{”÷}^{HIO_{4}}$RCHO+R”äCHO
$”ś_{”÷}^{HIO_{4}}$RCHO+R”äCHO
 £¬CCH3CHO£¬F
£¬CCH3CHO£¬F £®
£® +
+ $”ś_{”÷}^{ÅØĮņĖį}$
$”ś_{”÷}^{ÅØĮņĖį}$ +2H2O£®
+2H2O£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 2014Äź10ŌĀ£¬±±¾©”¢¹ž¶ū±õµČ¶ąøö±±·½³ĒŹŠ³öĻÖŃĻÖŲĪķö²ĢģĘų£¬¶ąĖłŃ§Š£±»ĘČĶ£æĪ£¬Ōģ³ÉĪķö²µÄ”°×ļæż”±Ö®Ņ»ŹĒĘū³µĪ²Ęų£®µ±½ńĘū³µĪ²Ęų“¦ĄķÖ÷ŅŖ¾ČżŌŖ“ß»ÆĘ÷“¦Ąķ£¬ĘäÖ÷ŅŖĪŪČ¾Īļ£ØCO”¢NOx£¬Ģ¼Ēā»ÆŗĻĪļ£©æÉ×Ō·¢µÄĻą»„·“Ó¦±ä³ÉĪŽŗ¦ĘųĢ壬¼õÉŁ»·¾³ĪŪČ¾£¬Ęä·“Ó¦ŌĄķÖ®Ņ»£ŗ2NO£Øg£©+2CO£Øg£©ØTN2£Øg£©+2CO£Øg£©”÷H£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
2014Äź10ŌĀ£¬±±¾©”¢¹ž¶ū±õµČ¶ąøö±±·½³ĒŹŠ³öĻÖŃĻÖŲĪķö²ĢģĘų£¬¶ąĖłŃ§Š£±»ĘČĶ£æĪ£¬Ōģ³ÉĪķö²µÄ”°×ļæż”±Ö®Ņ»ŹĒĘū³µĪ²Ęų£®µ±½ńĘū³µĪ²Ęų“¦ĄķÖ÷ŅŖ¾ČżŌŖ“ß»ÆĘ÷“¦Ąķ£¬ĘäÖ÷ŅŖĪŪČ¾Īļ£ØCO”¢NOx£¬Ģ¼Ēā»ÆŗĻĪļ£©æÉ×Ō·¢µÄĻą»„·“Ó¦±ä³ÉĪŽŗ¦ĘųĢ壬¼õÉŁ»·¾³ĪŪČ¾£¬Ęä·“Ó¦ŌĄķÖ®Ņ»£ŗ2NO£Øg£©+2CO£Øg£©ØTN2£Øg£©+2CO£Øg£©”÷H£¬»Ų“šĻĀĮŠĪŹĢā£ŗ| Ź±¼ä/s | 0 | 2 | 3 | 4 |
| C£ØNO0£Ø”Į10-4mol•L-1£© | 20.0 | 3.00 | 2.00 | 2.00 |
| C£ØCO£©£Ø”Į10-3mol•L-1£© | 2.70 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | äåŅŅĶéµÄµē×ÓŹ½ | |
| B£® | ĻņäåŅŅĶéÖŠµĪČėAgNO3ČÜŅŗ¼ģŃéĘäÖŠµÄäåŌŖĖŲ£ŗBr-+Ag+ØTAgBr”ż | |
| C£® | äåŅŅĶéÓėKOHČÜŅŗ·“Ó¦£ŗCH3CH2Br+H2O$”ś_{”÷}^{KOH}$C2H5OH+KBr | |
| D£® | ÓĆäåŅŅĶéÖĘČ”ŅŅ¶ž“¼¾¹żŅŌĻĀ¼ø²½£ŗĻūČ„”ś¼Ó³É”śĖ®½ā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
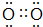 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH2=CH-CH2-CH3ŗĶ | B£® |  Óė Óė | ||
| C£® | ·Ö×Ó×é³É¶¼ĪŖ CnH2nO2 µÄĪļÖŹ | D£® | CH3CH2ClÓėCH3CH2CH2Cl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HSO3-ŌŚČÜŅŗÖŠ·¢ÉśĖ®½ā£ŗHSO3-+H2O?SO32-+H3O+ | |
| B£® | ĻņNaClOČÜŅŗÖŠĶØČėÉŁĮæSO2£ŗ2ClO”„+SO2+H2OØTSO32”„+2HClO | |
| C£® | ±½·ÓÄĘČÜŅŗĻŌ¼īŠŌ£ŗC6H5O-+H2O?C6H5OH+OH- | |
| D£® | ¶čŠŌµē¼«µē½āMgCl2ČÜŅŗ£ŗCl-+2H2O$\frac{\underline{\;µē½ā\;}}{\;}$ OH-+Cl2”ü+H2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŹÆ»ŅĖ® | B£® | CO | C£® | ŃĪĖį | D£® | C2H5OH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com